Перейти к:
Нефрология: фундаментальная и клиническая
https://doi.org/10.24884/1561-6274-2019-23-4-9-26
Аннотация
В настоящее время фундаментальная нефрология включает в себя многие разделы смежных наук, дающих новый импульс к пониманию механизмов функционирования почки на молекулярном уровне. Авторы статьи подчеркивают, что в основе функций почек лежат молекулярные системы, включающие разнообразные рецепторы, котранспортеры, насосы и ионные каналы, которые в конечном итоге обеспечивают гомеостаз организма. Фундаментальная нефрология, представляющая собой синтез физиологии и молекулярных ОМИКС-исследований, позволяет врачу более глубоко вникать в сущность патологических процессов, проводить диагностику болезней почек на доклиническом уровне. Тесная взаимосвязь фундаментальной и клинической нефрологии обеспечивает не только трансляцию научных достижений в практику, но и способствует персонификации терапии.
Ключевые слова
Для цитирования:
Смирнов А.В., Наточин Ю.В. Нефрология: фундаментальная и клиническая. Нефрология. 2019;23(4):9-26. https://doi.org/10.24884/1561-6274-2019-23-4-9-26
For citation:
Smirnov A.V., Natochin Yu.V. Nephrology: fundamental and clinical. Nephrology (Saint-Petersburg). 2019;23(4):9-26. (In Russ.) https://doi.org/10.24884/1561-6274-2019-23-4-9-26
ВВЕДЕНИЕ
Нефрология как самостоятельная дисциплина сформировалась во второй половине XX в. Выделилось направление клинической нефрологии [1, 2, 3], появились первые руководства, периодические издания [4, 5]. Проблемы нефрологии касаются широкого круга вопросов, включая строение почки, ее функции, развитие, регуляцию функций, фармакологию почек и т.п. Обычно в руководствах по нефрологии состояние каждого из этих разделов науки рассматривается в отдельных главах [3, 4]. Очевидно, что в реальных условиях in vivo процессы, происходящие в почке, как и в ином органе живого существа, могут быть поняты при осмыслении их морфофункциональной организации, регуляции, действия на них физиологически активных веществ, фармакологических средств, молекулярной организации функций.
Понимание природы физиологических явлений в почке, неизбежно должно рассматриваться в тесной связи с состоянием организма, знанием их предыстории, выяснения возможных дисфункций работы почек, что будет естественным образом раскрываться в клинической нефрологии. Сказанное позволяет заключить, что нефрология как наука должна включать два раздела: фундаментальную нефрологию и клиническую нефрологию.
Фундаментальная нефрология представляет собой целостную систему знаний, включающую морфологию (анатомия, гистология, ультраструктура), эмбриологию, физиологию, биохимию, молекулярную биологию, иммунологию, фармакологию почек. В каждом из упомянутых разделов должны быть учтены проблемы развития, биологии, взаимозависимости при построении целостных систем. Принципиально важным является разграничение понятий 1) о процессах, лежащих в основе мочеобразования, и 2) о функциях почек в организме [6]. Это имеет особое значение для клинициста, поскольку симптомы находят выражение в дисфункциях почки, а их природа, понимание механизмов функции основаны на количественной оценке каждого из процессов, обусловливающих мочеобразование.
ФУНДАМЕНТАЛЬНАЯ НЕФРОЛОГИЯ
Вехи нефрологии
Термин «нефрология» в медицинской литературе появился впервые, по-видимому, в средине XX в. [1, 4]. Следует в нескольких словах разграничить термины, казалось бы, близкие в их англоязычном выражении, но имеющие разные оттенки смыслового значения и используемые в нашей статье. Фундаментальный - fundamentalis, (лат. яз.), означает лежащий в основании [7], в английском языке - принцип, основной, существенный [8]. Фундаментальная нефрология включает формулирование ключевых представлений о структуре и функции почек на основе данных морфологии, физиологии, биохимии, генетики, иммунологии почек. Разное прочтение будут в строгом смысле слова иметь словосочетания - «основы нефрологии» и «основа нефрологии» - Fundamental nephrology и Fundamentals nephrology. На эти, казалось бы, малозаметные отличия следует обратить внимание. В первом случае речь идет о духе нефрологии, ее базовых принципах, во втором - о комплексе знаний, касающихся интеграции данных о почке в норме и патологии.
Четко обозначим проблему обсуждения - 1) накопление знаний о структуре, функции почек, болезнях почек и 2) формирование нефрологии как научной дисциплины. Если знания, касающиеся первой из упомянутых проблем, накапливались более двух тысячелетий, то возраст второй проблемы скромнее и насчитывает несколько десятилетий. Вехами в формировании нефрологии можно считать появление первых руководств, монографий, периодических изданий, научных обществ, в названии которых использовалось слово «нефрология». В некоторых случаях может быть названа точная дата, подчеркнем, речь идет не о книгах, посвященных различным аспектам деятельности почек и их болезней, а именно о нефрологии.
Первый конгресс Международного общества нефрологов состоялся во Франции, в Эвиане в 1960 г., второй - в Чехословакии, в Праге в 1963 г., третий - в 1966 г. в США, в Вашингтоне. Наша страна была представлена уже на II Международном конгрессе нефрологов, Европейских коллоквиумах по физиологии почек, в редколлегиях Kidney Int., Renal Failure и др. В 60-е годы ХХ в. стали формироваться нефрологические общества в разных странах. Американское общество нефрологов было основано в 1966 г., его первое собрание состоялась 18-19 октября 1967 г. в Калифорнии, в Лос-Анджелесе. В СССР учредительное собрание Общества нефрологов прошло в декабре 1969 г. в Европейской гостинице, присутствовало 12 человек. Заседание проводил акад. АМН СССР Е.М. Тареев, представителями от Ленинграда были А.Я. Ярошевский и Ю.В. Наточин. Первый съезд нефрологов СССР состоялся в Минске с 1 по 4 октября 1974 г. под председательством Е.М. Тареева. В 1972 г. были изданы Основы нефрологии в 2 томах под редакцией Е.М. Тареева [3]. В этом руководстве имеются главы по основным разделам нефрологии: морфологии почек, физиологии почек, методам диагностики, классификации болезней почек, основным нозологическим формам и др. В числе первых руководств по нефрологии был том Nephrology, изданный под редакцией Амбурже и др. [4]. В книге представлены главы по анатомии, эмбриологии и физиологии почек, главные синдромы, болезни почек, их лечение, трансплантация.
Была разработана единая классификация структур почки [9], изданы руководства, в которых обобщены данные о функциях почек [10], болезнях почек [11, 12]. В нашей стране изданы руководства и монографии по различным аспектам изучения структуры, функции почек, клиники болезней почек [3, 13, 14], появились руководства по педиатрической нефрологии [15-19]. Появилось несколько периодических изданий журналов - «Нефрология», «Нефрология и диализ», «Клиническая нефрология».
Среди тех, кто интересуется проблемами нефрологии, несравненно больше занимающихся клинической, чем фундаментальной нефрологией. Безусловно, требуется развитие не только обеих сторон этой науки, но и очевидна взаимная польза такого союза. Для фундаментальной нефрологии клиническая нефрология имеет важное значение в проверке верности ее выводов, она служит и источником новых вопросов. В свою очередь, клиническая нефрология использует достижения фундаментальной нефрологии, базовые знания для понимания патогенеза, дифференциальной диагностики, разработки новых лекарственных средств и методов обследования, глубокого проникновения в логику развития патологических процессов.
Таблица 1 / Table 1
Функции, дисфункции почки и процессы мочеобразования
Kidney functions, dysfunctions and urinary processes
Функции | Дисфункции | Фильтрация | Реабсорбция | Секреция | Синтез |
|---|---|---|---|---|---|
Осморегуляция | Гипоосмоляльнось, гиперосмоляльность | + | + |
|
|
Волюморегуляция | Отеки | + | + |
|
|
Регуляция pH | Ацидоз, алкалоз | + | + | + |
|
Ионорегулирующая | Гипокалиемия, гиперкалиемия и др. | + | + | + |
|
Метаболическая | Дизметаболизм | + | + | + | + |
Инкреторная | Гипертензия, анемия, остеопороз и др. |
|
|
| + |
Экскреторная | Уремия | + | + | + |
|
Примечание. Объяснение в тексте.
Функции почек и механизм мочеобразования
Дидактическое значение такого подхода в клинической физиологии почек - рассмотрение 1) функций почек и 2) процессов мочеобразования, предложенное нами почти полвека назад, имеет значение для лучшего понимания роли почек в организме и клинической нефрологии. Назначение почек в организме определяется выполняемыми ими функциями. Вспомним, что вскоре после применения гемодиализа стало ясно, что представление о почке только как об органе выделения ущербно, у пациентов на диализе стали наблюдаться многие симптомы, обусловленные нарушениями из-за того, что не возмещаются некоторые функции почек помимо выделения конечных продуктов обмена веществ. Перечислим функции почек, чтобы охарактеризовать многогранность их роли в организме. Участие почек в осморегуляции обеспечивает стабилизацию важнейшего физико-химического параметра крови во имя поддержания постоянного объема каждой клетки. Волюморегулирующая функция почек лежит в основе сохранения объема крови и внеклеточной жидкости. Почки участвуют в регуляции концентрации каждого из ионов в сыворотке крови, поддержании кислотно-основного равновесия - pH крови, что обусловливает саму возможность функционирования клеток. Мало было известно об участии почек в обмене белков, липидов, углеводов в организме (метаболическая функция), а эта функция определяет роль почек в синтезе глюкозы, строгой проверки качества белков сыворотки крови. Инкреторная функция почек обусловливает секрецию эритропоэтина, ренина, тромбопоэтического фактора, активных форм витамина D3 и многих гормонов. Экскреция конечных продуктов азотистого обмена, избытка углеводов, аминокислот, различных ионов хорошо известна. В основе осуществления этих функций почек лежат 4 процесса: гломерулярная фильтрация; канальцевая реабсорбция; канальцевая секреция; синтез веществ в структурах почки (табл. 1). Приведенное выше разграничение между функциями почек и процессами, лежащими в основе мочеобразования, позволяет подойти к проблеме компенсаторных возможностей, вовлечь иные функциональные системы для возмещения утраченных функций или повышения эффективности лечения.
Серьезной проблемой фундаментальной нефрологии является выяснение состояния организма пациента и его отражения в симптомах, в данных лабораторного или инструментального исследования. В интегральной оценке состояния пациента неоценимое значение принадлежит опыту и интуиции клинициста, существенное значение имеют не только данные анализа, но и их интерпретация. В повседневном анализе оценивается клиренс креатинина. Чаще всего ныне он стал не расчетной величиной, а определяемой по стандартной формуле, где ключевое значение имеет концентрация креатинина в сыворотке крови. При таком подходе следовало бы принимать во внимание повседневный рацион, степень развития мышечной массы у пациента и т.п. Приходится встречаться с грубейшими ошибками, когда представляют показатели клиренса креатинина в расчете на 70 кг массы тела и приводят значения 200-250 мл/мин. Очевидно, что такая величина клубочковой фильтрации не может быть, так как у человека кровоснабжение почки достигает исключительно высоких значений - 25 % крови, поступающей в минуту в аорту, а чтобы обеспечивать более высокий уровень клубочковой фильтрации, необходимо было бы изменить это соотношение. Подобный анализ может быть применен к другим стандартным методам обследования, а исключительное значение имеет истинное понимание принципов работы почки, ее полифункциональности.
Естественно, что фундаментальная наука является основой любого раздела естествознания и прикладных направлений науки. Эти проблемы были детально проанализированы ранее, и внимание было сосредоточено на достижениях сопредельных наук, которые определяют развитие нефрологии [19]. Помимо устоявшихся представлений в фундаментальной нефрологии важно коснуться тех сторон деятельности почек, которые требуют переосмысления. Фундаментальная нефрология предполагает и постановку новых задач, совместную их разработку физиологами с клиницистами и на этой основе более глубокое понимание процессов, происходящих и в почке, и в организме пациента в зависимости от клинической картины. Созданные физиологами и применяемые в клинике методы количественной оценки состояния почек, данные о нормальных величинах позволяют достаточно точно определить скорость гломерулярной фильтрации, величину почечного кровотока, значение реабсорбции или секреции веществ в почке. Имеющиеся подходы дают картину состояния иммунонефрологии, эндокринной функции почек. Количественные показатели касаются начального этапа мочеобразования, основанного на ультрафильтрации и результата (экскреция) как следствия реабсорбции и секреции веществ.
Фундаментальная нефрология дала клинической нефрологии возможность реальной количественной оценки процессов, лежащих в основе мо- чеобразования, проникновения в природу отклонения от нормы функций почки. Методы клиренса, техника биопсии позволили оценивать состояние почек при разных формах патологии, назначать лечение, адекватно характеризовать стадии болезни. Разработана система клинико-физиологического обследования, которая позволяет выявлять состояние и резервные возможности почек.
Фундаментальная нефрология - это преобразование установленных, обоснованных статических картин о роли каждого из процессов, обеспечивающих образование мочи, в динамическую картину реальной деятельности почек в организме здорового или больного человека. Новые данные показывают, что даже в условиях нормальных значений клубочковой фильтрации и величины диуреза системы регуляции могут менять объем и состав содержимого в одном из отделов нефрона, и тогда иное количество жидкости поступит в следующие отделы канальца. Если возрастет реабсорбция ионов Na в проксимальном сегменте нефрона и толстом восходящем отделе петли Генле, то иное количество ионов поступит в область macula densa, незамедлительно наступит реакция в виде усиления секреции ренина с известными последствиями. При стабильной гломерулярной фильтрации уменьшение реабсорбции Na+ и Cl- в толстом восходящем отделе петли Генле приведет при наличии в крови вазопрессина к увеличению реабсорбции осмотически свободней воды в сочетании с полиурией, несмотря на стабильность скорости клубочковой фильтрации. Увеличение в крови глюкагоноподоб- ного пептида-1 [20] или окситоцина [21] вызывает снижение проксимальной реабсорбции, а от того и изменение функций дистального сегмента нефро- на, в итоге - мочеотделения. Следовательно, внимание клинициста должно быть привлечено при оценке функционального состояния почек к базовым параметрам КФО, их возможной динамике, вызванной функциональным состоянием пациента или развивающимся патологическим процессом.
Рассмотрим некоторые сложные проблемы фундаментальной нефрологии, которые либо не ставились в литературе, либо не нашли ясного решения. Почка человека обеспечивает разные грани гомеостаза [22], в учебниках и общественном сознании почка относится к главным органам выделения. В почках человека в сутки ультрафильтрации в клубочках подвергается около 180 л жидкости, из которых реабсорбируется более 178 л, в норме выделяется менее 1,5-2 л мочи. В сосуды почек в сутки поступает более 1200 л крови, что составляет четверть минутного объема сердца. Следует ответить на фундаментальный вопрос, почему природа выбрала столь энергетически затратный способ работы почек, а не экскрецию ненужных веществ за счет секреторного аппарата клеток.
В новейшей литературе по нефрологии внимание сосредоточено на молекулярных механизмах функциональной активности почек и у здорового человека, и при разных формах патологии. Исследования с применением методов молекулярной биологии и молекулярной генетики существенно изменили облик современной науки, нефрологии в том числе. Уже несколько десятилетий разрабатывается молекулярная физиология почек, которая позволяет понять, каким образом осуществляется каждая из функций почек. В то же время все меньше стало выполняться работ с использованием системного подхода, с проникновением в суть тех функциональных преобразований, которые основаны на отдельных молекулярных процессах не только в клетках канальца, но того или иного сегмента нефрона и почки в целом.
Новые данные фундаментальной нефрологии позволяют пересмотреть значение отдельных сегментов нефрона и архитектуры почек. Стала ясна огромная роль проксимального сегмента нефрона, поскольку на смену существовавшим со второй половины XIX в. и в течение XX в. представлениям об облигатной реабсорбции жидкости в проксимальном сегменте нефрона человека, млекопитающих животных она оказалось регулируемой при участии глюкагоноподного пептида-1, ангитензина, окситоцина. Следствием регуляторного уменьшения проксимальной реабсорбции служит возрастание притока жидкости в дистальный сегмент нефрона и иные эффекты фармакологических средств на процесс мочеобразования.
Требует клинического осмысления проблема нового понятия, которое названо нами «функциональные петли нефрона». Хорошо известна роль петли Генле в осмотическом концентрировании мочи [12]. Имеется еще несколько функциональных петель в почке, возникающих, естественно, на иной структурной основе, которые играют важную роль в процессе мочеобразования. Состояние гломерулярной фильтрации определяется тем, как происходит реабсорбция Na+ и Cl- в проксимальном канальце и восходящем отделе петли Генле, эти изменения воспринимаются рецепторами в области юкстагломерулярного аппарата каждого нефрона - клетками macula densa в момент прохождения жидкости, и это вызывает изменение скорости секреции ренина в данном клубочке. Применение лекарственных средств типа эксенатида и функционально подобных ему препаратов при лечении сахарного диабета 2-го типа вызывает уменьшение проксимальной реабсорбции, и меняется деятельность функциональной петли, включающей проксимальный сегмент нефрона и толстый восходящей отдел петли Генле. Естественно, эти процессы могут по-разному происходить в разных популяциях нефронов, тем более при разных формах патологии. Следует упомянуть о функциональной петле между толстым восходящим отделом дистального сегмента нефрона и собирательной трубкой. Ее клетки реагируют на десмопрессин, диклофенак, меняется реабсорбция Na+, Cl-, воды, что находит отражение в измененной секреции простагландинов, вовлечении аквапорина 2, что выявляется в эксцессах ночного энуреза у детей [23].
Большая трудность в работе клинициста-нефролога состоит и в том, что в каждом из процессов, лежащих в основе мочеобразования, участвует много факторов регуляции, а надо найти ведущий именно у данного пациента, что затрудняет выбор стратегии лечения, например, при гипертензии. Можно привести много примеров, которыми богата фундаментальная нефрология в ее тесной связи с клинической нефрологией. Среди функций почки важное значение имеет участие почек в метаболизме органических веществ в организме, например, в белковом обмене. Измененные белки, в отличие от здоровых, проходят гломерулярный фильтр, поступают в проксимальный извитой каналец, реабсорбируются его клетками, в них эти белки гидролизуются до аминокислот, дипептидов и возвращаются в кровь для построения новых белков. Эта функция почек сыграла неоценимую роль у жителей блокадного Ленинграда, когда был скудный рацион, голод, и в организме происходило уникальное явление перераспределения белков. Многие клетки подверглись апоптозу, разрушению, фрагменты измененных белков фильтровались в клубочках, в клетках проксимального канальца осуществлялся их гидролиз, а аминокислоты поступали в кровь и шли на восстановление клеток жизненно важных органов, прежде всего мозга и сердца. Судя по архивным данным, сменился и характер патологии почек в годы блокады. Эта же функция реализуется повседневно у здоровых и больных, но она в клинике может иначе отражаться и иметь иную симптоматику при парентеральном питании, перегрузке проксимального канальца фильтруемым белком.
Фундаментальная нефрология вводит нас в мир новых понятий, которые безусловно требуют совместимости с классическими представлениями о работе почек. Генотип человека установлен в химических терминах великих достижений XX в., каждый человек уникален, он обладает своим вариантом генотипа - фенотипом. На этой основе формируется морфологическая основа каждого человека, она обусловливает физико-химический матрикс для деятельности клеток, органов, систем человека, диктует условия проявления дисфункции при патологии у данного пациента. Эта матрица каждое мгновение формирует все новые узоры соотношения молекул регуляторов, влияющих на рецепторы, локализованные в плазматической мембране или в субструктурах клетки. Это мириады процессов, управление или понимание их организации у здорового, а тем более больного человека - необычайно сложная задача. Для проникновения в святая святых ее работы требуется глубокое исследование организации данной системы. Современное естествознание, современная физиология в обзорах, руководствах, многотомных учебниках дают возможность понять элементы осуществления функций отдельных систем: кровообращения, дыхания, пищеварения, выделения. Но это приводит к необходимости постановки более общих вопросов, на которые пока нет ответа и которые недавно поставлены. Их суть в том, как установлен стандарт основных физико-химических параметров у человека - стандарт температуры тела, осмоляль- ности жидкостей внутренней среды, концентрации каждого из ионов. Где в организме находится, как организован единый центр, обеспечивающий целостность организма, его «Я» [24]. Это позволило бы подойти к вопросу об отклонениях в условиях патологии, особенно при разных клинических состояниях, поиску путей восстановления, а быть может выбора оптимального варианта «нормы» для разных стадий болезни и у реконвалесцентов. В клинике нередко развивается без явных причин субфебрилитет, в чем механизм перестройки центра регуляции температуры тела?
В этой связи следует упомянуть о достижениях фундаментальной нефрологии последних десятилетий, когда были выявлены варианты подтипов рецепторов для одного и того же гормона. В частности, для основного регулятора объема выделяемой почкой мочи - вазопрессина - известны 3 подтипа рецепторов: V1a, V1b, V2. Все они представлены в плазматических мембранах клеток канальцев, но они могут быть стимулированы в люминальной или базолатеральной мембране, они расположены в разных отделах нефрона, они вовлекают в последующие реакции разные вторичные мессенджеры. V2-рецепторы, регулируют проницаемость канальца для воды, усиливают реабсорбцию Na+, V^-рецепторы угнетают реабсорбцию Na+, V^-рецепторы стимулируют секрецию K+ и его выделение почкой.
Этим отнюдь не завершается перечень эффектов вазопрессина при участии тех же рецепторов этого гормона у человека и млекопитающих животных. Они участвуют в свертывании крови, влияя на концентрацию VIII фактора, вазопрес- син обладает выраженным действием на поведение, эмоциональную сферу человека [25]. Не продолжая перечень влияния факторов регуляции, следует прийти к заключению об огромном значении особенностей фенотипа и сиюминутных, реализуемых каждое мгновение действий систем регуляции, палитра которых, наблюдаемая и непрестанно сменяемая их мозаика требует нового клинического мышления, нового подхода, и не подвластны шаблонам, стандартному пониманию.
Ключевой проблемой для нефрологии становится то, что стало именоваться трансляционной медициной. Данные фундаментальной нефрологии должны становиться не фигурой речи, а способом диагностики или лечения [26, 27, 28]. Однако возникает зачастую ситуация, не допускающая однозначного механического ответа. Причин много, одна из них в существовании компенсаторных реакций, параллельных метаболических путях. Можно выразить сомнение, что ее быстро решит искусственный интеллект. Скорей предположить, что опыт клинициста, поможет при обследовании выявить трудно формализуемые микросимптомы и это приблизит к точному диагнозу, верному прогнозу и верной стратегии лечения.
Молекулярная нефрология в клинике
В последние годы были разработаны методы анализа молекулярного состава биологических образцов (клетка, ткань, биологические жидкости - кровь, моча и пр.), экспресс-методы определения нуклеотидной последовательности ДНК и РНК. В их числе микроэррей-технология (микро- чипирование ДНК, РНК), лазерная микродиссек- ция, MALDI-Tof; MSI-матрично-активированная лазерная десорбция - с времяпролетным анализом; визуализирующей масс-спектрометрией; спектроскопия ядерно-магнитного резонанса высокого разрешения, капиллярный электрофорез и др. [29]. Использование этих технологий с применением компьютерных программ обработки больших массивов данных, применение системного подхода с построением безмасштабных сетей взаимодействия [30] позволило перейти от исследования одного гена, РНК, белка, метаболита к интегральному изучению генома, транскрип- тома, протеома, метаболома, липидома. В литературе укоренился новый термин, объединяющий названные разделы (геномика, транскриптомика, протеомика и т.д.) как ОМИКС-исследования.
Уместно сделать отступление, касающееся общей методологии проведения таких исследований. При классическом подходе сначала созревает идея, формируется общая гипотеза и цель исследования, ставятся задачи исследования и формулируются частные гипотезы. В ОМИКС-исследованиях формируется только общая цель - извлечь наиболее полный набор данных (ассоциации генов, РНК, белков, метаболитов) при какой-либо патологии. Далее осуществляется компьютерная обработка данных в рамках системного подхода и полученные результаты подвергают анализу. Такой путь напоминает обработку больших массивов разнородных данных в информатике, получивший название Data Mining. В литературе классический научный подход иногда называют таргетным (англ., target - мишень, адресный, целевой), а ОМИКС- исследования именуют нетаргетными. Заметно сходство нетаргетного исследования с обследованием, о котором шла речь вначале, однако то, что дозволено в экспериментальных исследованиях с применением индукции, вряд ли возможно в дедуктивных областях, к которым относится клиническая медицина, нефрология в частности.
Геномика. Настоящим прорывом в генетических исследованиях мультифакториальных заболеваний (в том числе в нефрологии) для выявления «генов предрасположенности» явилось создание на основе новых технологий метода полногеномного анализа ассоциаций (ПГАА) (Genove Wide Association Studies - GWAS). Суть метода ПГАА заключается в применении ДНК-биочипов (микроэррей-анализ) высокой плотности, которые позволяют осуществлять одновременно типирование тысячи и более SNP-сайтов. Полученные данные на популяции с конкретным заболеванием сравнивают с базой данных международного проекта Нар Мар (гаплоидная карта), содержащей сведения о распределении тысячи полиморфных сайтов - однонуклеотидных замен и карты гаплотипов - устойчивых сочетаний вариаций однонуклеотидного полиморфизма. В результате идентифицируются все возможные однонуклеотидные полиморфизмы, ассоциированные с изучаемой формой патологии [31, 32]. К реальным успехам применения ПГАА в нефрологии можно отнести ассоциацию гена APOL1 с фокальносегментарным гломерулосклерозом (ФСГС) и терминальной почечной недостаточностью (ТПН) у афроамериканцев [33], гена МУН9 с ФСГС, ВИЧ- ассоциированной нефропатией, с ТПН вследствие гипертензивной нефропатии [34, 35], трех генов ядерных пор (NUP93, NUP205, XPO5) со стероид- резистентными нефротическим синдромом [36]. С помощью ПГАА было выявлено наличие взаимосвязей между общим однонуклеотидным полиморфизмом в восходящей области гена уромодулина (UMOD) с состоянием экскреторной функции почек и артериальной гипертензией [37, 38]. Результаты ПГАА гена UMOD внесли значительный вклад в понимание механизмов вовлечения уро- модулина (белка Тамма-Хорсфалла) в механизмы регуляции функции почечных канальцев, баланса натрия и артериального давления. Это может стать основой создания подходов к лечению артериальной гипертензии. В результате выполнения ПГАА у здоровых людей было установлено, что аллели гена UMOD, ассоциированные с низким содержанием белка Тамма-Хорсфалла в моче (rs 12917707, rs 4293393, rs 13333226), соотносятся с более высокими значениями скорости клубочковой фильтрации [37, 38], что может объяснять вариацию ее величин у здоровых [39].
Успехи геномики при изучении болезней почек очевидно станут основой предсказательной нефрологии, когда наряду с клиническими данными (возраст, пол, анамнез и др.) и особенностями генотипа человека можно будет формировать группы риска пациентов в отношении патологии почек. Геномные исследования могут сыграть большую роль в определении нозологической принадлежности и в оценке течения и прогноза заболевания. Примером может служить гематология, где детекция аномальных генов является обязательным условием для постановки диагноза ряда гемобластозов. Выявление специфических транслокаций и мутаций имеет значение при анализе течения заболевания, его прогноза и в выборе терапии. Однако в нефрологии пока идет накопление материала для оценки перспектив реального применения геномики. Следует принять во внимание вариабельность генетического полиморфиза в разных популяциях. Выявленная ассоциация может быть связана не с самим геном- кандидатом, а с геном, который ответственен за синтез протеина, компенсирующего деятельность мутантного гена (эпистатическое взаимоотношение генов). Патогенез заболевания может быть обусловлен нарушением системы взаимодействий не одной, а нескольких генных сетей [31]. В связи с этим имеют перспективу постгеномные технологии, которые дают возможность оценивать результаты эспрессии генов на различных уровнях: матричные и другие РНК (транскриптомика), протеины и их посттрансляционные модификации (протеомика), метаболиты (метаболомика).
Транскриптомика. Суть транскриптомики заключается в инвентаризации РНК с помощью технологии микрочипов с последующим проведением высокопроизводительного секвенирования нуклеотидов [40]. Объектом для транскриптомики служат отдельные клетки или ткани. В нефрологии используются биоптаты почки. С этой целью создаются международные биобанки биологических образцов тканей (нефробиоптаты), биологических жидкостей (кровь, моча). В начале XXI века был создан Европейский банк ДНК (The Consorcium of European Renal c DNA Bank). В США организована Северо-Американская многоцентровая сеть изучения нефротического синдрома (NEPTUNE). В этом банке хранятся нефробиоптаты от взрослых и детей с различными гломерулопатиями (БМИ, ФСГС, МН) для установления корреляций клинических и лабораторных показателей с данными транcкриптомики [41]. Пока идет накопление материала, касающегося отдельных сторон патогенеза гломерулопатий. Так, при IgA-нефропатии определена роль одного из цитокинов активированного врожденного иммунитета в происхождении гематурии [42] и значения гиперактивации Wnt-β- катенинового пути в патогенезе этой нефрологической патологии [43]. При волчаночном нефрите в результате индивидуализированного иммуномониторинга транскриптома крови были установлены молекулярные сети, позволяющие стратифицировать пациентов на 7 групп [44]. У пациентов с АНЦА-ассоциированным олигоиммунным гломерулонефритом с полулуниями с помощью транскриптомного анализа биоптатов была выявлена гиперэкспрессия СС-хемокинового лиганда 18. Авторы полагают, что данная молекула может претендовать на роль биомаркера активности и рецидива болезни [45]. После накопления данных при исследовании образцов биоптатов биобанка при различных гломерулопатиях можно будет говорить о составлении цельной сети молекулярных взаимодействий (интерактом), что в свою очередь откроет перспективы для разработки таргетных препаратов.
Отдельный раздел транскриптомики связан с изучением микро-РНК (ми-РНК), которые участвуют в механизмах эпигенетической регуляции деятельности генов: их активации (экспрессии) или угнетении (репрессии). Ми-РНК вовлечены в регуляцию множества различных биологических процессов - пролиферацию, дифференциацию, апоптоз, канцерогенез [46, 47]. Для микро-РНК характерна специфическая экспрессия в разных тканях и клетках. Микро РНК: 146а; 886; 192; 194; 204; 215 и 216 являются для почек специфичными, а микро-РНК: 196 а/в; 10 а/в; 130; 146, 200а, 30а-е; 872; 21-высокоспецифичными [48]. Наиболее адекватным методом исследования ми-РНК является микроэррэй-анализ, поскольку он позволяет выявить одновременно спектр ми-РНК в биологическом образце (моча, ткань почки, кровь) [49]. Экспрессия отдельных видов ми-РНК может определяться при помощи реакции амплификации (Real-time PCR-протокол). При остром повреждении почек (ОПП) описано более 50 различных ми-РНК [50]. Экскреция почкой ми-РНК-21 и ми- РНК-494 увеличивается в несколько раз на ранних стадиях ОПП еще до повышения уровня креати- нина крови, что позволяет рассматривать их в качестве ранних маркеров этого состояния [51, 52]. С помощью ПГАА ми-РНК мононуклеаров периферической крови пациентов с IgA-нефропатией было установлено, что гиперэкспрессия ми-РНК 148 в В-лимфоцитах может быть ответственна за процесс гликозилирования IgA1, который, как известно, является главным фактором в патогенезе нефропатии [53]. Мочевая экскреция ми-РНК 204, 431, 555 при IgA-нефропатии снижена, а ми-РНК 150 - значительно повышена по сравнению с контрольной группой здоровых лиц. Наибольшее диагностическое значение (чувствительность - 56 %, специфичность - 100 %>) при IgA-нефропатии имеет уровень мочевой экскреции ми-РНК 204 [54]. Предварительные данные говорят о том, что уровень экспрессии некоторых ми-РНК (142-5р; 155) в нефробиоптатах трансплантата позволяет надежно предсказывать острую реакцию отторжения [37, 38].
Протеомика. Протеомика изучает белковый состав различных биологических сред, структурнофункциональные свойства белковых молекул. У пациентов с аутоиммунными первичными и вторичными гломерулопатиями исследуются кровь, моча и паренхима почки, полученная путем прижизненной нефробиопсии. В протеомном анализе используют методы обратно-фазовой жидкостной хроматографии высокого давления и высокого разрешения, масс-спектрометрию (MALDI/ионизация). Как правило, при проведении протеомного анализа используют комбинацию этих двух методов [57]. Основная цель протеомного анализа состоит в изучении биологических образцов (кровь, моча, ткань). После выявления белкового спектра, производится идентификация отдельных белков при сравнении с международными базами данных физико-химических свойств белков и структуры генома [57]. По результатам анализа могут быть отобраны наиболее характерные для данного патологического состояния белки-представители, которые далее могут использоваться как биомаркеры в клинической практике при иммунохимическом или иммуноферментном методах определения. Так, например, применена таргетная техника протеомного анализа с использованием аптамерной технологии у пациентов с хронической болезнью почек (ХБП) различных стадий [40]. Было выделено 813 протеинов, из них 60 биомолекул могли претендовать на роль биомаркеров ХБП [58]. Интересно отметить, что два белка из 60 хорошо знакомы нефрологам - это цистатин-С и β2-микроглобулин. Эти два белка используются в клинической практике для оценки функционального состояния почек, гломерулярной фильтрации и степени поражения проксимальных канальцев. Для определения их концентрации в биологических средах разработаны иммунофер- ментные методы, что значительно упрощает работу клинициста. Протеомика паренхимы почки, полученная с помощью нефробиопсии, позволяет выявить изменения в белковом спектре при различных заболеваниях почек, что имеет большое дифференциально-диагностическое значение. Проведению собственного протеомного анализа предшествует лазерная микродиссекция, позволяющая исследовать гломерулы, тубулоинтерстиций. С помощью лазерной микродиссекции с последующей MALDI/ионизацией или SOMA-сканирования были дифференцированы такие гломерулопатии, как мембрано-пролиферативный гломерулонефрит, AL-амилоидоз, криоглобулинемический, фибриллярный и иммунотактоидный гломерулонефриты [59, 60]. Протеомный анализ почек сыграл решающую роль в открытии М-типа рецептора фосфолипазы А2 (PLA2R) в качестве аутоантигена при идиопатической мембранозной нефропатии [61]. Данный рецептор регулирует эффекты фос- фолипазы А2, вызывая активацию или торможение разнообразных биологических реакций [62].
При проведении протеомного анализа гломерулярного компартмента почечной паренхимы, выделенного с помощью лазерной микродиссекции с последующим применением масс-спектрометрии, была получена белковая фракция с множеством различных белков, которая при сравнении с базой данных белков человека была сведена к 18 возможным кандидатам на аутоантиген. Далее с помощью моноклональных антител и рекомбинантных белков был идентифицирован белок PLA2R [63]. Затем был осуществлен полногеномный поиск ассоциаций на европейской выборке пациентов с идиопа- тической МН. В результате были установлены две аллельные ассоциации: с HLA-DQA1 и с PLA2R [64]. Эти исследования позволили модифицировать наши представления о патогенезе МН. Полагают, что у генетически предрасположенных лиц, обладающих аллелью HLA-DQA1, может происходить изменение конформации (структуры) PLA2R под влиянием внешних неблагоприятных факторов (токсины, лекарственные средства, вирусы, бактерии), что приводит к появлению аутоантигенности PLA2R и обусловливает продукцию анти-PLA2R- аутоантител [62, 65]. Aнти-PLA2R-аутоантитела обнаруживаются не менее чем у 70 % пациентов с идиопатической МН и могут служить для мониторинга активности заболевания, оценки эффективности терапии и прогноза [66]. Аутоантигенный статус пациентов с идиопатической мембранозной нефропатией в 30 % случаев оставался неизвестным вплоть до последнего времени, если не считать редкие неонатальные варианты МН обусловленного аутоантителами к подоцитарной нейтральной эндопептидазе (NEP, нефролизин) [62]. В 2014 году Tomas N.M. и соавт. [67] обследовали 15 пациентов с анти-PLA2R-негативным вариантом идиопатической МН. С помощью вестерн-блоттинга был выделен неизвестный гломерулярный белок с молекулярной массой 250 KDa. Далее с помощью масс-спектрометрии он был идентифицирован как домен тромбоспондина 1-го типа, содержащий 7А (THSD7A) [67]. Антитела к THSD7A, полученные от пациентов с идиопатической МН, при введении лабораторным мышам вызывали развитие типичного поражения клубочков [68]. Антитела к THSD7A выявляются у 10 % пациентов с идиопатической МН. Однако пока не существует серийно выпускаемых наборов для определения циркулирующих аутоантител к THSD7A [62].
Таким образом, протеомика почек, как раздел фундаментальной нефрологии, формирует для клинициста своеобразное «окно» в молекулярные механизмы патогенеза гломерулопатий. Протеом- ный анализ мочи имеет особенности, поскольку нативная моча содержит не только низко-, но и высокомолекулярные белки, а также микровезикулы (экзосомы) и апоптотические тельца, происходящие из различных отделов нефрона. В связи с этим образцы мочи требуют преданалитической подготовки: удаление крупномолекулярных протеинов (например, белка Тамма-Хорсфала) с помощью аффинной хроматографии, проведение ультрацентрифугирования в сахарозном градиенте плотности с целью изоляции экзосом и микрочастиц. Далее образец мочи подвергается фракционной фильтрации с целью получения двух фракций, содержащих белки с молекулярной массой более 4KDa (для исследования протеома) и менее 4KDa (для исследования пептидома и метаболома) [69]. Получение белковых фракций может осуществляться с применением различных методов (вестерн-блоттинг, капиллярный электрофорез и др.), а их идентификация устанавливается с помощью масс-спектрометрии [70]. M. Haubitz и соавт. (2005) при исследовании протеома мочи пациентов с первичными гломерулопатиями выделили 28 белков, которые позволили дифференцировать IgA-нефропатию и идиопатическую МН с чувствительностью 77 % и специфичностью 100 % [71]. Протеом мочи успешно использован для дифференциальной диагностики волчаночного нефрита, идиопатической МН, диабетической нефропатии и фокально-сегментарного гломерулосклероза [72].
Современные клинические представления о дисфункции почек были обобщены в наднозо- логическом понятии хронической болезни почек (ХБП) [73]. Для ее диагностики используют такие показатели, как альбуминурия, расчет скорости клубочковой фильтрации (СКФ), который отражает выраженность дисфункции почек. Однако СКФ позволяет лишь приближенно оценивать дисфункцию почек. Альбуминурия может отсутствовать, несмотря на персистирующую прогрессию гломеруло- и тубулоинтерстициального склероза, морфологического субстрата терминальной почечной недостаточности [74]. В связи с этим были предприняты попытки оценить протеом мочи с целью более точной и ранней диагностики ХБП. Классическим в этом отношении стало исследование D.M. Good и соавт. (2010), которые выполнили протеомный анализ мочи с применением капиллярного электрофореза и масс-спектрометрии у 273 пациентов с ХБП различной этиологии в сравнении с протеомом мочи 379 здоровых людей [75]. Идентификацию белков спектра осуществляли, сравнивая результаты со сведениями из международной базы данных (Structured Query Language data base), включающей 5010 образцов протеинов с молекулярной массой от 800 до 1700 Da из мочи 3600 человек. В результате было идентифицировано 273 белка, которые с высокой достоверностью позволяли дифференцировать пациентов с ХБП от контрольной группы здоровых лиц. Данное исследование легло в основу создания классификатора белков протеома мочи при ХБП (CКD273-классификатор). В последующих исследованиях было установлено, что данный классификатор CKD273 на ранних стадиях ХБП (СКФ=70-80 мм/мин/1,73) значительно лучше, чем альбуминурия, характеризует повреждение почечной паренхимы [76] и может быть использован для дифференциации отдельных нозологических форм гломеру- лопатий (МН, ФСГС, IgA-нефропатия, БМИ, СКВ, диабетическая нефропатия, васкулиты) [77].
Протеомный анализ мочи, который дает результаты высокой надежности и достоверности, иногда называют «жидкостной биопсией». Конечно, протеомика мочи не сможет отменить не- фробиопсию в ближайшем будущем, но при уже установленном морфологическом диагнозе позволит осуществлять динамическое наблюдение за процессами, происходящими в ткани почек - активностью воспалительного процесса, фибро- зированием; позволит вовремя диагностировать обострение или вхождение пациента в ремиссию [78]. Протеомный анализ позволяет также выделить среди общего белкового спектра тех представителей, которые в наибольшей степени характерны для той или иной патологии, стадии патологического процесса, развития фиброзирования (биомаркеры). Для этих протеинов создаются более простые методы их определения (иммунофер- ментные или иммунохимические), которые удобны для применения в клинике у постели пациента. В настоящее время существует большое число таких биомаркеров (NGAL, KIM-1, NAG, LFABP, ИЛ-18 и мн. др.), которые доказали эффективность при диагностике ранних стадий острого [79, 80] и хронического [81, 82] повреждения почек.
Метаболомика. Последовательность ОМИКС- исследований в молекулярной нефрологии завершает метаболомика. Метаболизм тесно связан с фенотипом [83] и способен адекватно отражать функционирование отдельных органов и организма в целом, реагировать на влияние внешней среды (диета, токсины, лекарства и др.). Идея использовать особенности метаболического профиля для диагностики различных болезней была предложена Л. Полингом еще в 1971 году. Проанализировав выдыхаемый воздух методом газовой хроматографии при различных заболеваниях, они выявили более 200 различных химических субстанций органической природы [84]. Термин метаболом или метаболический профиль означает совокупность веществ с низкой молекулярной массой (<1500Da), являющихся промежуточными или конечными продуктами обмена веществ, которые могут быть идентифицированы в отдельных клетках, тканях или биологических жидкостях (кровь, моча, спинномозговая жидкость) [85]. В настоящее время создана база данных метаболома человека, которая включает более 100 000 метаболитов различного происхождения (ткани, биожидкости, клетки) и спектра с референсными значениями их концентраций [86, 87]. Аналитическая платформа метаболических исследований - это жидкостная хроматография, масс-спектрометрия или спектроскопия ядерного магнитного резонанса (ЯМР- спектроскопия) [88, 89]. Смысл современной метаболомики заключается в том, что в каком бы звене цепи геном-транскриптом-протеом не произошли изменения, они не могут не сказаться на интенсивности метаболических процессов в клетке, тканях, органе, организме. К генетически предопределенным факторам следует добавить воздействие внешней среды (диета, лекарства, токсины) и патологические состяния, такие как ишемиче- ски/реперфузионное повреждение, воспаление (микробное, иммунное, вследствии воздействия самих метаболитов, например, мочевой кислоты при подагре), дегенеративные изменения (атеросклероз, гликированные продукты, свободные радикалы, фиброзирование, апоптоз). Эти процессы касаются и нефрологической клиники - ишемия/ реперфузия при остром повреждении почек, ишемия почки при атеросклерозе почечной артерии, ишемия тубулоинтерстиция при гломерулосклерозе, аутоиммунное воспаление при гломерулопати- ях и тубулоинтерстициальных нефритах, фиброзирование и склерозирование при ХБП и формировании терминальной почечной недостаточности. Можно предположить, что при перечисленных процессах метаболизм почки может нарушаться, что в конечном счете скажется на обмене веществ организма. При изучении метаболома мочи при IgA-нефропатии были выявлены пять летучих метаболитов (тартроновая кислота, карбаминовая кислота, сульфид-амил-метил-гидроксил-азид, бензенэтанамин, пентафлюорофенил-метилен) в более высокой концентрации по сравнению с метаболо- мом мочи у пациентов с мембранопролиферативным гломерулонефритом [90]. В некоторых исследованиях были идентифицированы метаболиты в моче, которые коррелировали с протеинурией, причем наибольшие изменения были связаны с тяжестью течения заболевания, отмечались в метаболическом пути фенилаланина [91]. Своеобразие метаболического профиля биологической среды при патологии находит отражение в характерной «метаболической подписи» в моче, она выявлена при IgA-нефропатии, идиопатической МН [92] и в плазме крови при волчаночном нефрите [93, 94].
КЛИНИЧЕСКАЯ НЕФРОЛОГИЯ
Фундаментальная и клиническая нефрология взаимно формируют общие представления и единый подход к оценке происходящих в организме человека патологических процессов. Фундаментальная нефрология позволяет познать сущность болезни, вскрыть базовые законы ее возникновения и развития, лежит в основе теоретических представлений, которые у постели пациента укладываются в дедуктивные рассуждения о природе субъективных и объективных (физикальных, лабораторных, инструментальных) симптомов. Не случайно термин «симптом» (symptom, греч.) означает совпадение. Внешнее, наблюдаемое или регистрируемое, при осмыслении врачом должно «совпасть» с внутренним (структурой, функцией, в итоге патогенезом), составляющим суть симптома, в его современном понимании. Субстрат подавляющего числа нефрологических симптомов (как субъективных, так и объективных) представлен той или иной дисфункцией (парциальной, органной или организменной): артериальная гипертензия, отеки, повышение концентрации креатинина, снижение скорости клубочковой фильтрации, глюкозурия при нормальном уровне глюкозы в крови, полиурия, никтурия и т.д. Часть симптомов представлена морфологическим субстратом: микрогематурия, альбуминурия (протеинурия), увеличение размеров почек, выявленных при ультразвуковом исследовании (нефросарка при нефротическом синдроме), и др.
От анализа симптома и формирования обоснованного предположения о его субстрате (семиоло- гическая дифференциальная диагностика) клиницист переходит к выделению комплекса симптомов на основании их патогенетической связи, совокупности (синдром), к диагностике конкретной нозологической единицы (болезни) среди нескольких, которые могут существовать в рамках данного синдрома (нозологическая дифференциальная диагностика). Как известно, такой путь диагностики носит название «от симптома к синдрому, и от него к диагнозу» и представляет собой классический научно-исследовательский метод работы клинициста у постели больного. В России он был сфомулирован и введен в практику С.П. Боткиным в конце XIX века [95], а за рубежом в начале ХХ века У Ослером. Задача статьи не только раскрыть клинико-физиологический метод диагностики по С.П. Боткину, но и показать неразрывную связь клинической и фундаментальной нефрологии, продемонстрировать необходимость этой кооперации при исследовании пациента для постановки диагноза у данного пациента. С нашей точки зрения, назрела острая потребность в широком применении подобного подхода, так как в последние годы при обучении специалистов (студентов) в практическом здравоохранении все энергичнее декларируется принцип всестороннего обследования пациента при постановке диагноза, а не сочетания с исследованием. Обследование - это инспектирование объекта, тестирование организма пациента с надеждой, что будут выявлены специфические черты, признаки чего-то, что позволит поставить диагноз.
В итоге возникает субъективная убежденность врача и организаторов здравоохранения в том, что «диагноз ставит» компьютерная томография, биопсия почки, лабораторные данные и др. Напротив, истинное, глубокое исследование всегда лежит в основе организованного с определенного целью и целенаправленного познания. Постановка диагноза определяется клинической симптоматикой, ее анализом, связью с предполагаемым субстратом (морфологическим или дисфункциональным), что обусловливает назначение дальнейших методов обследования (лабораторных и инструментальных). Таким образом, примениние методов исследования, включая самые современные и технически сложные, определяется не столько схемами, стандартами или протоколами, а мыслью, идеей, гипотезой врача-клинициста- исследователя на базе фундаментальной науки. В основе такой научно-исследовательской деятельности врача-нефролога, конечно, лежат материалы, положения, достижения и теории фундаментальной нефрологии. Изложенный способ клинической диагностики, методология работы клинициста, составляют основу его клинического мышления в сочетании с интуицией, к этому за годы работы прибавляется практический опыт. Резким контрастом к вышеизложенным подходам служит метод диагностики по набору симптомов, по аналогии с уже виденным или по образцу наставлений (учебник, стандарт, протокол), по жестким данным наиболее современных и «специфичных» методов исследования (которых, как правило, не оказывается в данный момент в конкретном лечебном учреждении. «А вот, если бы они имелись, тогда-то...», - сетуют клиницисты).
Однако никакие, даже новейшие, методы исследования (о которых речь впереди) не заменяет глубокой мысли, последовательной логики Врача. Выдающийся клиницист Г.И. Сокольский, говоря о системе клинического мышления, еще в первой трети XIX века писал: «Способ изучения медицины не должен разниться от способа изучения других естественных наук. Каждая наука имеет только свои материалы (содержания), но способ рассматривания оных совершается по тем же законам разума, кои общи каждой голове, хотя и не в равной степени» [96]. Клиницист-нефролог в повседневной деятельности не открывает новых болезней, не устанавливает доселе неизвестных механизмов ее развития и тем не менее, применяя методологию научного исследования, всегда отвечает не только на вопрос «что это?», но и на вопросы «как и почему?», «почему так, а не иначе?». О таком истинно фундаментальном подходе говорили, писали А. Эйнштейн в 1929 г. [97] и Л.А. Орбели в 1956 г. [98] Ответы на последние вопросы позволяют клиницисту преобразовывать абстрактное понятие «болезнь» в индивидуальный подход, привести его в соответствие с особенностями данного конкретного пациента с учетом возраста, пола, наследственности, перенесенных болезней, реактивности организма, сопутствующих заболеваний и т.д. Очевидно, что выполнить эту задачу, не обладая определенной суммой знаний фундаментальной нефрологии, невозможно и, напротив, применение знаний фундаментальной науки к конкретному пациенту наполняет работу клинициста творчеством, делает ее успешной, приносящей удовлетворение, пользу пациенту и обеспечивает профилактику профессионального «выгорания». «Ядром клинического мышления является способность к мысленному построению синтетической и динамической картины болезни, к переходу от восприятия явлений заболевания к воссозданию ее «внутреннего» течения, патогенеза. Развитие «умственного видения», умение включить любой симптом в логическую цепь своих рассуждений - важнейшее качество клинициста» [99].
В научно-популярной литературе и в художественных произведениях часто касаются темы медицины, науки и искусства. Зачастую высказываются мнения прямо противоположные, но большинство соглашается с представлением о том, что медицина - это «искусство, основанное на науке» [100]. При этом под «искусством» чаще всего понимается мастерство и ремесло (в лучшем смысле этого слова), что бесспорно для большинства «хирургических» специальностей. Однако практически никто не говорит об «искусстве мышления» у постели пациента. Можно предполагать, что «мышление» автоматически включается в понятие научной медицины, но удивительно то, что фундаментальный подход при этом связывают с достижениями в тех областях, которые служат клинике, обеспечивая обследование пациента (молекулярная биология, физиология, компьютерные технологии и мн. др.), т.е. выступают лишь в роли инструмента научно-исследовательской деятельности врача у постели пациента.
Распространенным является мнение, что современная медицина «вышла за пределы формальной диагностики, на которую опирались предыдущие столетия, и больше не гадает по косвенным признакам о причинах заболевания - теперь они выявляются напрямую!!» [101]. Эта цитата приведена не с целью полемики с автором, а потому, что она отражает мнение многих современных врачей и организаторов здравоохранения. Постараемся разобраться в проблеме вдумчиво. Дело в том, что как во времена М.Я. Мудрова, Г.И. Сокольского, Г.И. Захарьина, С.П. Боткина, Е.М. Тареева и других выдающихся клиницистов, так и в современной практике никто не «гадал по косвенным признакам о причинах заболевания». Диагноз болезни устанавливался по совокупности субъективных и объективных симптомов, увязанных в единую и логически непротиворечивую систему на основе тех фундаментальных механизмов понимания патологического процесса, его патогенеза, которые существовали в то время. Уровень теоретического знания и понимания болезни (патологического процесса) определял и нозологические критерии. В нефрологии недалекого прошлого до внедрения в клинику прижизненной нефробиопсии (конец 50-х, начало 60-х годов ХХ столетия) представление о нефритах, их классификация и нозологические критерии базировалось на клинической картине болезни: острый, подострый или злокачественный и хронический нефриты. Морфология патологического процесса не включалась в нозологические критерии, т.к. могла быть проанализирована только при аутопсии. Тем не менее клиницист E. Volhard и патолог T. Fahr на основании изучения аутопсийных биоптатов почки создали классификацию, которая включала нефриты, нефрозы и нефро склероз почек [102]. Термин «нефроз» E. Volhard и T. Fahr заимствовали из более ранней работы E. Muller (1905), который, в свою очередь, предложил его взамен термина «паренхиматозный нефрит» (предложенный Р. Вирховым (Virchow R., 1863) для характеристики «невоспалительного, неэкссудативного» процесса в паренхиме почки [103].
В клинике в то время чаще употребляли термин «липоидный нефроз» (как синоним нефроза), впервые предложенный F. Munk в 1913 году на основании того, что в моче пациентов с липоидным нефрозом находили в значительном количестве жировые тельца [103]. Термин «гломерулонефрит» предложил еще в 1872 Klebs T., но он использовался значительно реже, чем термин «нефрит». Полагали (и не без оснований), что патологический процесс охватывает не только клубочек, но и межуточную ткань [103]. Термин «нефроз» связывали с первичным поражением канальцев, а не клубочков. В наши дни, как известно, в клинике используется термин «нефротический синдром», который в отличие от нефроза подразумевает первичное повреждение клубочка (подоцитопатии - болезнь минимальных изменений, фокальносегментарный гломерулосклероз, мембранозная нефропатия) с вторичными изменениями канальцев. В доантибиотиковую эру в общей структуре болезней почек преобладал постстрептококковый нефрит (гломерулонефрит), который протекал тяжело с выраженными отеками, в том числе головного мозга и легких. Доминировала концепция, что стрептококк является единственным этиологическим фактором гломерулонефрита, а хронический гломерулонефрит всегда является исходом острого, который своевременно не был диагностирован. Не имея возможности прижизненной морфологической диагностики, использовались клинические критерии, которые, как казалось в то время, были способны отразить индивидуальные особенности в течении гломерулонефрита как цельной и единой патологии. Так появилась классификация, подразделяющая хронический гломерулонефрит на латентный, нефротический, гипертонический, гематурический, гипертонически-нефротический и др., которые трактовались как формы единой нозологической единицы - гломерулонефрита [104]. Удивительно, что и в наше время подобные диагнозы еще встречаются в нефрологических отделениях, и пациенты получают небезопасную терапию глюкокортикоидами и цитостатиками, которую назначают, по сути, на основании нозологических критериев середины ХХ века.
Со времени широкого внедрения прижизненной нефробиопсии нозологические критерии гломеру- лонефрита стали морфологическими. В настоящее время выделяют пролиферативные и непролиферативные варианты гломерулонефрита (табл. 2).
Таблица 2 / Table 2
Пролиферативные и непролиферативные морфологические формы гломерулопатий
Proliferative and non-proliferative morphological forms of glomerulopathy
Тип гломерулопатии | Морфологические формы гломерулонефрита | |
|---|---|---|
Пролиферативные (гломерулонефриты) | Непролиферативные (гломерулопатии, нефропатии) | |
Первичные (идиопатические) | • IgA-гломерулонефрит • Мембранопролиферативный гломеруло- нефрит • Анти-ГБМ-нефрит* (синдром Гудпасчера) | • Болезнь минимальных изменений • Фокально-сегментарный гломерулосклероз • Мембранозная нефропатия • Наследственные варианты нефротического синдрома (мутации генов протеинов щелевидной диафрагмы) • Синдром Альпорта • Болезнь тонкой базальной мембраны • Болезнь Фабри |
Вторичные | • Постинфекционные гломерулонефриты** • Волчаночный нефрит • Системные васкулиты мелких сосудов*** | • Амилоидоз • Болезнь отложения легких и тяжелых цепей иммуноглобулинов • Диабетическая нефропатия • Медикаментозная мембранозная нефропатия |
Примечание. * - гломерулонефрит, обусловленный аутоантителами к антигену гломерулярно-базальной мембраны; ** - включая постстрептококковый гломерулонефрит; *** - обусловленные иммунными комплексами (криоглобулины, опухолевые антигены, ревматоидный артрит и др.), антителами к цитоплазме нейтрофилов (синдром Вегенера, микроскопический полиангиит, синдром Чарджа-Штроса).

Рис. 1. Иммуноморфологи- ческая дифференциальная диагностика мембранопролиферативного гломеру- лонефрита (МБПГН)
Figure 1. Immunomorphological differential diagnosis of membrane-proliferative glomerulonephritis
Примечание: + Состав иммуноглобулинов различный и в определенной степени зависит от этиологии основного заболевания. Наряду с С3-фракцией могут выявляться C1q-, С2-, С4-фракции, определенно свидетельствующие о классическом пути активации комплемента; ++ Могут выявляться следовые количества иммуноглобулинов (2+), обычно в зонах склероза, не имеющие диагностического значения; * Присутствует только С3-фракция, фракции C1q, С2, С4 не выявляются (альтернативный путь активации комплемента); ** Репаратив- ная фаза может имитировать МБПГН; *** Термин «болезнь плотных депозитов» является предпочтительным. Не рекомендуется употреблять термин «МБПГН II типа».
Первые характеризуются выраженной экссудацией и пролиферацией в клубочке (лейкоциты, макрофаги, лимфоциты, резидентные клетки клубочка), а при непролиферативных вариантах воспалительные признаки в гломерулах отсутствуют, что объясняется тем, что иммунный процесс локализуется кнаружи от базальной гломерулярной мембраны в субподоцитарном пространстве, в связи с чем провоспалительные цитокины и хемо- кины не имеют доступа к резидентным клеткам клубочка (эндотелиоциты, мезангиоциты) и не в состоянии обеспечить хемотаксис лейкоцитов. Таким образом, единая, как казалось ранее, болезнь в виде хронического гломерулонефрита распалась на несколько форм нозологии. Пролиферативные варианты гломерулонефрита могут клинически проявлять себя в острой, хронической форме или приобретать быстропрогрессирующее течение, если пролиферация выходит за пределы капилляров и вовлекает эпителий капсулы Боумена с образованием так называемых полулуний. Непролиферативные варианты гломерулонефрита клинически презентируются нефротическим синдромом вследствие структурных изменений подоцитов, ножковые отростки которых со щелевидной диафрагмой между ними в норме являются преградой для проникновения белка в мочевое пространство. Несмотря на то, что современные нозологические критерии гломерулонефрита стали морфологическими, клинические симптомы гломерулярной патологии и сама клиническая диагностика никуда не исчезли, просто симптомы получили детальную морфологическую интерпретацию. Более того, представления о морфопатогенезе пролиферативных вариантов гломерулонефрита позволили сгруппировать симптомы в синдромы - острый нефритический, быстропрогрессирующий нефритический и хронический нефритический синдромы, которые ранее принимались за нозологические единицы. Данный подход отражен в международной классификации болезней 10 пересмотра. Методы иммунофлюоресценции и иммуногистохимии с использованием моноклональных антител к различным классам иммуноглобулинов, их тяжелым и легким цепям, а также к отдельным фракциям комплемента (C1q,C3; C4d и др.) позволили нефрологам глубже проникнуть в патогенез пролиферативных гломерулопатий. Мембрано-пролиферативный гломерулонефрит, который до этого считался патогенетически единым нозологическим вариантом, распался на иммунокомплексный (иммуноглобулин- и С3-комплемент позитивный вариант), на гломерулонефрит, обусловленный активацией альтернативного пути комплемента (иммуноглобулиннегативный, С3-комплемент позитивный) и на неиммунный вариант, при котором отсутствуют отложения иммуноглобулинов и фракций комплемента и который отмечается в исходе такого заболевания, как тромботическая микроангиопатия (рис. 1) [105].
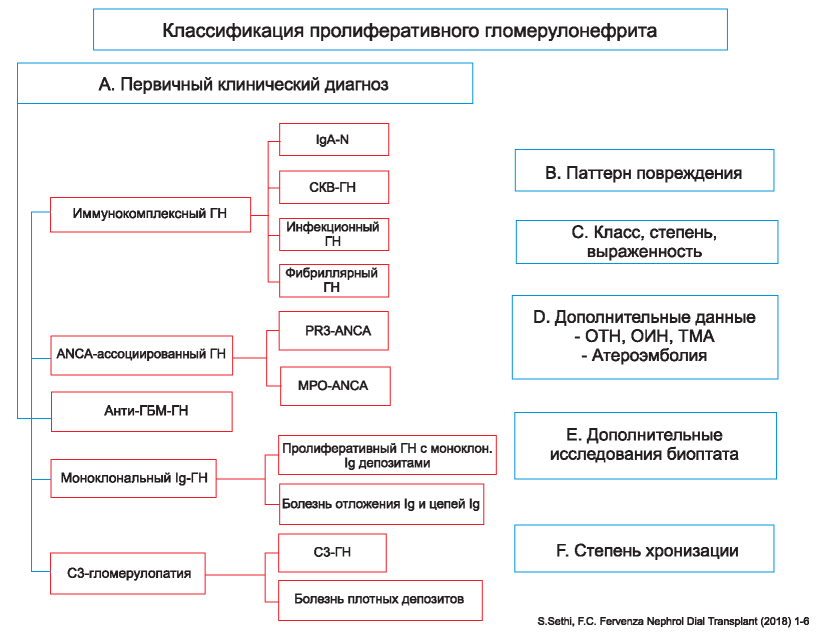
Рис. 2. Классификация пролиферативного гломерулонефрита.
Figure 2. Classification of proliferative glomerulonephritis
В ходе накопления клинического материала становилось все очевиднее, что морфологические признаки того или иного варианта пролиферативного гломерулонефрита являются результирующими разных патогенетических механизмов и с этой точки зрения исполняют лишь роль паттерна, своеобразного «морфологического синдрома». В литературе появились предложения классифицировать пролиферативные варианты гломерулонефрита не только по морфологии (паттерну повреждения), но и в соответствии с ведущим иммунным механизмом, а также отражать в диагнозе степень выраженности морфологических изменений, хронизацию процесса и указывать дополнительные данные, которые могут оказывать влияние на клинику заболевания (поражение канальцев, тубулоинтерстиция, капилляров) (рис. 2) [106].
Сейчас трудно сказать, насколько приемлемой и востребованной в практической работе окажется данная классификация, но примечателен сам факт динамики клинических представлений в соответствии с новыми данными фундаментальной нефрологии.
Список литературы
1. Шик О. Нефрология практического врача. Гос. изд-во мед. лит., Прага, 1967, 341 с.
2. Виктор З. Клиническая нефрология. Польское государственное медицинское издательство, Варшава, 1968, 344 с.
3. Тареев ЕМ. Основы нефрологии. В 2-х томах. Медицина, М., 1972, 944 с.
4. Hamburger J, Crosnier J, Grunfeld JP. Nephrology. Wiley-Frammarion, New York, 1979, 1393 p.
5. Пелещук АП. Практическая нефрология. Здоров'я, Киев, 1973, 384 с.
6. Наточин ЮВ. Основы физиологии почки. Медицина, Л., 1982, 208 с.
7. Дворецкий ИХ. Латино-русский словарь. Русский язык, M. , 1986, 840 с.
8. Гальперин ИР. Большой англо-русский словарь в 2-х томах. Советская энциклопедия, М., 1972. Том 1, 823 с.
9. Kriz W, Bankir L, Bulger RE et al. A standart nomenclature for structures of the kidney. Kidney Int 1988;33(1):1-7
10. Smith HW. The Kidney: Structure and Function in Health and Disease. Oxford Univ. Press, New York, 1951,1049 p.
11. Brenner B (Еd.). Brenner & Rector's. The Kidney. 8 ed. Saunders Elsevier, Philadelphia, 2008 p.
12. Alpern RJ, Hebert SC (Eds.). Seldin andGeibisch's. The Kidney. Physiology and pathophysiology. Elsevier, Academic Press, Amsterdam, 2008, 1427 p.
13. Рябов СИ. Нефрология. СпецЛит, СПб, 2000, 672 с.
14. Шулутко БИ. Нефрология. Ренкор, СПб, 2002, 780 с.
15. Папаян АВ, Савенкова НД. Клиническая нефрология детского возраста. Левша, СПб, 2008, 600 с.
16. Папаян АВ, Стяжкина ИС. Неонатальная нефрология. Руководство. Питер, СПб, 2002, 238 с.
17. Эрман МВ. Нефрология детского возраста: руководство для врачей. 2 изд. СпецЛит, СПб, 2010, 683 с.
18. Игнатова МС. Детская нефрология. Руководство для врачей. 3-изд. МИЯ, М., 2011, 696 с.
19. Наточин ЮВ. Нефрология и фундаментальная наука. Нефрология 2012;16(1):09-21. doi: 10.24884/1561-6274-2012-16-1-9-21
20. Kutina AV, Golosova DV, Marina AS et al. Role of Vasopressin in the Regulation of Renal Sodium Excretion: Interaction with Glucagon-Like Peptide-1. J Neuroendocrinol 2016;28(4). doi: 10.1111/jne.12367
21. Наточин ЮВ, Голосова ДВ, Шахматова ЕИ. Новая функциональная роль окситоцина - участие в осморегуляции. Доклады Академии наук 2018;479(6):712-715
22. Наточин ЮВ. Гомеостаз. Успехи физиол. наук 2017;48(4):3-15
23. Natochin YuV, Kuznetsova AA. Nocturnal enuresis: correction of renal function by desmopressin and diclofenac. Pediatr Nephrol 2000;14:42-47
24. Наточин ЮВ. Целостность.Журн. высш. нерв. деятельности 2018;68(6):775-787
25. Шейман Дж. Патофизиология почки. Пер. с англ. Бином, М., 2019, 206 с.
26. Мухин НА. Нефрология: неотложные состояния. Эксмо, M., 2001, 288 с.
27. Эмануэль ВЛ. Лабораторная диагностика заболеваний почек. Тверь, СПб, 2006, 248 с.
28. Рябов СИ, Наточин ЮВ. Функциональная нефрология. Лань, СПб, 1997, 304 с.
29. Smith A, Galli M, L'Imperio V et al. MALDI-MS Imaging in the Study of Glomerulonephritis. Methods Mol Biol 2017;1618:85-94. doi: 10.1007/978-1-4939-7051-3_9
30. Смирнов АВ. Системный подход к анализу кардиоренальных взаимоотношений как первый шаг на пути к нефрологии формата П4. Нефрология 2011;15(2):11-19. doi: 10.24884/1561-6274-2011-15-2-11-19
31. Баранов ВС. Геномика на пути к предиктивной медицине. Acta Naturaen2009;3:77-89
32. Баранов ВС, Баранова ЕВ. Геном человека, эпигенетика многофакторных болезней и персонифицированная медицина. Биосфера 2012;4(1):76-85
33. Genovese G, Friedman DJ, Ross MD et al. Association of trypanolytic ApoL1 variants with kidney disease in African Americans. Science 2010;329(5993):841-845. doi: 10.1126/science.1193032
34. Friedman DJ, Pollak MR. Genetics of kidney failure and the evolving story of APOL1. J Clin Invest 2011;121(9):3367-3374. doi: 10.1172/JCI46263
35. Nelson GW, Freedman BI, Bowden DW et al. Dense mapping of MYH9 localizes the strongest kidney disease associations to the region of introns 13 to 15. Hum Mol Genet 2010;19(9):18051-815. doi: 10.1093/hmg/ddq039
36. Braun DA, Sadowski CE, Kohl S et al. Mutations in nuclear pore genes NUP93, NUP205 and XPO5 cause steroid-resistant nephrotic syndrome. Nat Genet 2016;48(4):457-465. doi: 10.1038/ng.3512
37. Kottgen A, Hwang SJ, Larson MG et al. Uromodulin levels associate with a common UMOD variant and risk for incident CKD. J Am Soc Nephrol 2010;21(2):3337-3344. doi: 10.1681/ASN.2009070725
38. Padmanabhan S, Melander O, Johnson T et al. Genomewide association study of blood pressure extremes identifies variant near UMOD associated with hypertension. PLoS Genet 2010;6(10):e1001177. doi: 10.1371/journal.pgen.1001177
39. Padmanabhan S, Graham L, Ferreri NR et al. Uromodulin, an emerging novel pathway for blood pressure regulation and hypertension. Hypertension 2014;64(5):918-923. doi: 10.1161/HYPERTENSIONAHA.114.03132
40. Дедов ИИ, Тюльпаков АН, Чехонин ВП и др. Персонализированная медицина: современное состояние и перспективы. Вестник Российской академии медицинских наук 2012;67(12):4-12. doi: 10.15690/vramn.v67i12.474
41. Gadegbeku CA, Gipson DS, Holzman LB et al. Design of the Nephrotic Syndrome Study Network (NEPTUNE) to evaluate primary glomerular nephropathy by a multidisciplinary approach. KidneyInt 2013;83(4):749-756. doi: 10.1038/ki.2012.428
42. Cox SN, Sallustio F, Serino G et al. Activated innate immunity and the involvement of CX3CR1-fractalkine in promoting hematuria in patients with IgA nephropathy. Kidney Int 2012;82(5):548-560. doi: 10.1038/ki.2012.147
43. Cox SN, Sallustio F, Serino G et al. Altered modulation of WNT-beta-catenin and PI3K/Akt pathways in IgA nephropathy. Kidney Int 2010;78(4):396-407. doi: 10.1038/ki.2010.138
44. Banchereau R, Hong S, Cantarel B. Personalized Immu-nomonitoring Uncovers Molecular Networks that Stratify Lupus Patients. Cell 2016;165(3):551-565. doi: 10.1016/j.cell.2016.03.008
45. Brix SR, Stege G, Disteldorf E et al. CC Chemokine Ligand 18 in ANCA-Associated Crescentic GN. J Am Soc Nephrol 2015;26(9):2105-2117. doi: 10.1681/ASN.2014040407
46. Ambros V. The functions of animal microRNAs. Nature 2004;431(7006):350-355. doi: 10.1038/nature02871
47. Бойко НВ, Голикова АЮ, Матишов ДГ, Тарасов ВА. Роль микроРНК в регуляции активности эукариот. Вестник Южного научного центра РАН 2011;7(3):69-78
48. Смирнов АВ, Карунная АВ, Зарайский МИ и др. Экспрессия микроРНК-21 в моче у пациентов с нефропатиями. Нефрология 2014;18(6):59-63
49. Thomson JM, Parker J, Perou CM, Hammond SM. A custom microarray platform for analysis of microRNA gene expression. Nat Methods 2004;1(1):47-53. doi: 10.1038/nmeth704
50. Fan PC, Chen CC, Chen YC et al. MicroRNAs in acute kidney injury. Hum Genomics 2016;10(1):29. doi: 10.1186/s40246-016-0085-z
51. Saikumar J, Hoffmann D, Kim TM et al. Expression, circulation, and excretion profile of microRNA-21, -155, and -18a following acute kidney injury. Toxicol Sci 2012;129(2):256-267. doi: 10.1093/toxsci/kfs210
52. Lan YF, Chen HH, Lai PF et al. MicroRNA-494 reduces ATF3 expression and promotes AKI. J Am Soc Nephrol 2012;23(12):2012-23. doi: 10.1681/ASN.2012050438
53. Serino G, Sallustio F, Cox SN et al. Abnormal miR-148b expression promotes aberrant glycosylation of IgA1 in IgA nephropathy. J Am Soc Nephrol2012;23(5):814-824. doi: 10.1681/ASN.2011060567
54. Szeto CC, Wang G, Ng JK et al. Urinary miRNA profile for the diagnosis of IgA nephropathy. BMC Nephrol 2019;20(1):77. doi: 10.1186/s12882-019-1267-4
55. Anglicheau D, Sharma VK, Ding R et al. MicroRNA expression profiles predictive of human renal allograft status. Proc Natl Acad Sci U S A 2009;106(13):5330-5335. doi: 10.1073/pnas.0813121106
56. Khan Z, Suthanthiran M, Muthukumar T et al. MicroRNAs and Transplantation. Clin Lab Med 2019;39(1):125-143. doi: 10.1016/j.cll.2018.10.003
57. Сучков СВ, Гнатенко ДА, Костюшев ДС и др. Про-теомика как фундаментальный инструмент доклинического скрининга, верификации анализов и оценки применяемой терапии. Вестник Российской академии медицинских наук 2013;68(1):65-71. doi: 10.15690/vramn.v68i1.540
58. Gold L, Ayers D, Bertino J et al. Aptamer-based multiplexed proteomic technology for biomarker discovery. PLoS One 2010;5(12):e15004. doi: 10.1371/journal.pone.0015004
59. Jain D, Green JA, Bastacky S et al. Membranoprolif-erative glomerulonephritis: the role for laser microdissection and mass spectrometry. Am J Kidney Dis 2014;63(2):324-328. doi: 10.1053/j.ajkd.2013.09.007
60. Sethi S, Theis JD, Vrana JA et al. Laser microdissection and proteomic analysis of amyloidosis, cryoglobulinemic GN, fibrillary GN, and immunotactoid glomerulopathy. Clin J Am Soc Nephrol 2013;8(6):915-921. doi: 10.2215/CJN.07030712
61. Mariani LH, Pendergraft WF 3rd, Kretzler M. Defining Glomerular Disease in Mechanistic Terms: Implementing an Integrative Biology Approach in Nephrology. Clin J Am Soc Nephrol 2016;11(11):2054-2060. doi: 10.2215/CJN.13651215
62. Бобкова ИН, Кахсуруева ПА, Ставровская ЕВ, Филатова ЕЕ. Эволюция в понимании патогенеза идиопатической мембранозной нефропатии: от экспериментальных моделей к клинике. Альманах клинической медицины 2017;45(7):553-564. doi: 10.18786/2072-0505-2017-45-7-553-564
63. Beck LH Jr, Bonegio RG, Lambeau G et al. M-type phospholipase A2 receptor as target antigen in idiopathic membranous nephropathy. N Engl J Med 2009;361(1):11-21. doi: 10.1056/NEJMoa0810457
64. Stanescu HC, Arcos-Burgos M, Medlar A et al. Risk HLA-DQA1 and PLA(2)R1 alleles in idiopathic membranous nephropathy. N Engl J Med 2011;364(7):616-626. doi: 10.1056/NEJMoa1009742
65. Ronco P, Debiec H. Pathophysiological advances in membranous nephropathy: time for a shift in patient's care. Lancet 2015;385(9981):1983-1992. doi: 10.1016/S0140-6736(15)60731-0
66. Добронравов ВА, Лапин СВ, Лазарева НМ и др. Циркулирующие антитела к рецептору фосфолипазы А2 при первичной мембранозной нефропатии. Нефрология 2012;16(4):39-44. doi: 10.24884/1561-6274-2012-16-4-39-44
67. Tomas NM, Beck LH Jr, Meyer-Schwesinger C et al. Thrombospondin type-1 domain-containing 7A in idiopathic membranous nephropathy. N Engl J Med 2014;371(24):2277-2287. doi: 10.1056/NEJMoa1409354
68. Tomas NM, Hoxha E, Reinicke AT et al. Autoantibodies against thrombospondin type 1 domain-containing 7A induce membranous nephropathy. J Clin Invest 2016;126(7):2519-2532. doi: 10.1172/JCI85265
69. Rovin BH, Klein JB. Proteomics and autoimmune kidney disease. Clin Immunol 2015;161(1):23-30. doi: 10.1016/j.clim.2015.04.021
70. Chen L, Su W, Chen H et al. Proteomics for Biomarker Identification and Clinical Application in Kidney Disease. Adv Clin Chem 2018;85:91-113. doi: 10.1016/bs.acc.2018.02.005
71. Haubitz M, Wittke S, Weissinger EM et al. Urine protein patterns can serve as diagnostic tools in patients with IgA nephropathy. Kidney Int 2005;67(6):2313-2320. doi: 10.1111/j.1523-1755.2005.00335.x
72. Varghese SA, Powell TB, Budisavljevic MN et al. Urine biomarkers predict the cause of glomerular disease. J Am Soc Nephrol2007;18(3):913-922. doi: 10.1681/ASN.2006070767
73. Levey AS, Eckardt KU, Tsukamoto Y et al. Definition and classification of chronic kidney disease: a position statement from Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int 2005;67(6):2089-100. doi: 10.1111/j.1523-1755.2005.00365.x
74. Miller WG, Bruns DE, Hortin GL et al. Current issues in measurement and reporting of urinary albumin excretion. Clin Chem 2009;55(1):24-38. doi: 10.1373/clinchem.2008.106567
75. Good DM, Zurbig P, Argiles A et al. Naturally occurring human urinary peptides for use in diagnosis of chronic kidney disease. Mol Cell Proteomics 2010;9(11):2424-2437. doi: 10.1074/mcp.M110.001917
76. Pontillo C, Mischak H. Urinary biomarkers to predict CKD: is the future in multi-marker panels? Nephrol Dial Transplant 2016;31(9):1373-1375. doi: 10.1093/ndt/gfv467
77. Siwy J, Zurbig P, Argiles A et al. Noninvasive diagnosis of chronic kidney diseases using urinary proteome analysis. Nephrol Dial Transplant 2017;32(12):2079-2089. doi: 10.1093/ndt/gfw337
78. Mischak H. Pro:urine proteomics as a liquid kidney biopsy: no more kidney punctures! Nephrol Dial Transplant 2015;30(4):532-537. doi: 10.1093/ndt/gfv046
79. Parikh CR, Mansour SG. Perspective on Clinical Application of Biomarkers in AKI. J Am Soc Nephrol 2017;28(6):1677-1685. doi: 10.1681/ASN.2016101127
80. Добронравов ВА, Смирнов КА, Афанасьев БВ и др. Острое повреждение почек и тубулярные биомаркеры при трансплантации гемопоэтических стволовых клеток. Терапевтический архив 2016;88(6):14-20. DOI: 10.17116/ terarkh201688614-20
81. Пролетов ЯЮ, Саганова ЕС, Галкина ОВ и др. Роль некоторых биомаркеров в оценке характера повреждения почек у пациентов с первичными гломерулопатиями. Нефрология 2013;17(1):60-69. doi: 10.24884/1561-6274-2013-17-1-60-69
82. Rysz J, Gluba-Brzozka A, Franczyk B et al. Novel Biomarkers in the Diagnosis of Chronic Kidney Disease and the Prediction of Its Outcome. Int J Mol Sci 2017;18(8). pii:E1702. doi: 10.3390/ijms18081702
83. German JB, Hammock BD, Watkins SM. Metabolomics: building on a century of biochemistry to guide human health. Metabolomics 2005;1(1):3-9. doi: 10.1007/s11306-005-1102-8
84. Pauling L, Robinson AB, Teranishi R, Cary P Quantitative analysis of urine vapor and breath by gas-liquid partition chromatography. Proc Natl Acad Sci U S A 1971;68(10):2374-2376. doi: 10.1073/pnas.68.10.2374
85. Xiao JF, Zhou B, Ressom HW. Metabolite identification and quantitation in LC-MS/MS-based metabolomics. Trends Analyt Chem 2012;32:1-14. doi: 10.1016/j.trac.2011.08.009
86. Wishart DS, Tzur D, Knox C et al. HMDB: the Human Metabolome Database. Nucleic Acids Res 2007;35(Database issue):D521-D526. doi: 10.1093/nar/gkl923
87. Wishart DS, Feunang YD, Marcu A et al. HMDB 4.0: the human metabolome database for 2018. Nucleic Acids Res 2018;46(D1):D608-D617. doi: 10.1093/nar/gkx1089
88. Фурина РР, Митракова НН, Рыжков ВЛ, Сафиуллин ИК. Метаболомические исследования в медицине. Казанский медицинский журнал 2014;95(1):1-6
89. Abbiss H, Maker GL, Trengove RD. Metabolomics Approaches for the Diagnosis and Understanding of Kidney Diseases. Metabolites 2019;9(2). pii:E34. doi: 10.3390/metabo9020034
90. Wang C, Feng Y Wang M et al. Volatile Organic Metabolites Identify Patients with Mesangial Proliferative Glomerulonephritis, IgA Nephropathy and Normal Controls. Sci Rep 2015;5:14744. doi: 10.1038/srep14744
91. Kalantari S, Nafar M, Samavat S, Parvin M. 1 H NMR-based metabolomics study for identifying urinary biomarkers and perturbed metabolic pathways associated with severity of IgA nephropathy: a pilot study. Magn Reson Chem 2017;55(8):693-699. doi: 10.1002/mrc.4573
92. Taherkhani A, Kalantari S, Arefi Oskouie A et al. Network analysis of membranous glomerulonephritis based on metabolomics data. Mol Med Rep 2018;18(5):4197-4212. doi: 10.3892/mmr.2018.9477
93. Guleria A, Pratap A, Dubey D et al. NMR based serum metabolomics reveals a distinctive signature in patients with Lupus Nephritis. Sci Rep 2016;6:35309. doi: 10.1038/srep35309
94. Li J, Xie XW, Zhou H et al. Metabolic profiling reveals new serum biomarkers of lupus nephritis. Lupus 2017;26(11):1166-1173. doi: 10.1177/0961203
95. Боткин СП. Курс клиники внутренних болезней и клинические лекции. В 2 томах. Медгиз, М., 1950. Том 1,364 с.
96. Смольянинов АВ, Хмельницкий ОК, Петленко ВП. Теоретические основы морфологического диагноза. СПбМАПО, СПб., 1995:13 [Smolyaninov AV, Khmelnitsky OK, Petlenko VP. The theoretical basis of morphological diagnosis. SPbMAPO, SPb., 1995:13 (In Russ.)]
97. Эйнштейн А. Цит. по: Марков М. О единстве и многообразии форм материи в физической картине мира. Наука и жизнь 1982;7:3-10
98. Орбели ИА. Избранные труды. В 2-х томах. Л., М., 1961. Том 1,61 с.
99. Смольянинов АВ, Хмельницкий ОК, Петленко ВП. Теоретические основы морфологического диагноза. СПбМАПО, СПб, 1995:12
100. Panda SC. Medicine: science or art? Mens Sana Monogr 2006;4(1):127-138. doi: 10.4103/0973-1229.27610
101. Разумов АС. Медицина XXI века: Биочипы. Медицина в Кузбасе 2009;2:3-11
102. Volhard F, Fahr Th. Брайтова болезнь почек. Перевод с нем. под редакцией Готье ЭВ, Мелких СМ. Белтрестпечать, Минск, 1923, 343 с.
103. Pal A, Kaskel F. History of Nephrotic Syndrome and Evolution of its Treatment. Front Pediatr 2016;4:56. doi: 10.3389/fped.2016.00056
104. Тареев ЕМ. Нефриты. Медгиз, М., 1958, 667 с.
105. Смирнов АВ, Добронравов ВА, Сиповский ВГ и др. Клинические рекомендации по диагностике, лечению и прогнозу мембранопролиферативного гломерулонефрита. Нефрология 2014;18(6):82-93
106. Сети C, Фервенца ФК. Стандартизированный подход к классификации и морфологическому описанию гломерулонефрита. Нефрология 2019;23(4)
Об авторах
А. В. СмирновРоссия
Смирнов Алексей Владимирович – профессор, доктор медицинских наук, директор научно-исследовательского института нефрологии, заведующий кафедрой пропедевтики внутренних болезней с клиникой.
197022, Санкт-Петербург, ул. Льва Толстого, д. 17, Тел.: (812)3386901
Ю. В. Наточин
Россия
Наточин Юрий Викторович - академик РАН, профессор, главный научный сотрудник Лаборатории физиологии почки.
194223, Санкт-Петербург, проспект М. Тореза, д. 44, Тел.: (812)5523086Рецензия
Для цитирования:
Смирнов А.В., Наточин Ю.В. Нефрология: фундаментальная и клиническая. Нефрология. 2019;23(4):9-26. https://doi.org/10.24884/1561-6274-2019-23-4-9-26
For citation:
Smirnov A.V., Natochin Yu.V. Nephrology: fundamental and clinical. Nephrology (Saint-Petersburg). 2019;23(4):9-26. (In Russ.) https://doi.org/10.24884/1561-6274-2019-23-4-9-26
JATS XML









































