Перейти к:
Растворимые рецепторы трансферрина и ферритиновый индекс в оценке метаболизма железа у диализных пациентов
Аннотация
Ключевые слова
Для цитирования:
Лапина Е.С., Батюшин М.М. Растворимые рецепторы трансферрина и ферритиновый индекс в оценке метаболизма железа у диализных пациентов. Нефрология. 2016;20(5):50-54.
For citation:
Lapina E.S., Batiushin M.M. Soluble transferrin receptor and ferritin index in evaluation of iron metabolism in hemodialysis patients. Nephrology (Saint-Petersburg). 2016;20(5):50-54. (In Russ.)
ВВЕДЕНИЕ
Хроническая болезнь почек (ХБП), в том числе ее терминальная стадия, рассматриваются как важная медико-социальная проблема, что обусловлено их значительной распространенностью, высокой стоимостью лечения, риском развития осложнений, смертностью [1-3]. Анемия является одним из наиболее распространенных осложнений ХБП и, согласно современным данным, наблюдается у каждого второго больного (47%), при этом ее частота обратно соотносится со степенью снижения скорости клубочковой фильтрации (СКФ) [4].
Патогенетические механизмы анемии при ХБП многочисленны, однако, ведущая роль принадлежит дефициту образования гликопротеидного ростового фактора эритроцитов — эритропоэтина и истощению доступного для эритропоэза пула железа [4, 5]. При этом феррокинетика представляет сложную систему взаимодействия ряда регуляторных механизмов, транспортных белков, депо-форм, значение которых и взаимосвязи активно изучаются, дополняясь новыми данными [6]. Так, в исследованиях продемонстрировано, что поступление железа в клетку осуществляется при взаимодействии комплекса железо-трансферрин со специфическим мембранным рецептором, который экспрессируется большинством клеток организма, но преимущественно клетками эритрона (80%) [7]. Пополнение внутриклеточного пула железа приводит к повышению синтеза ферритина для создания депо и уменьшению образования рецептора трансферрина в результате воздействия внутриклеточных регуляторных белков на мРНК ферритина и рецептора трансферрина. Соответственно в условиях дефицита железа запускается обратная реакция: повышение продукции специфического рецептора и снижение синтеза ферритина. Подобный ответ отмечается при активации эритропоэза, в том числе и на стимулирующее действие эритропоэтином [8]. Также для оценки обмена железа может быть использован интегративный показатель - ферритиновый индекс, расчет которого осуществляется исходя из уровня растворимых рецепторов трансферрина и ферритина в сыворотке крови. Указанный индекс рассматривается как лабораторный критерий для дифференциальной диагностики абсолютного и функционального дефицитов железа в рамках железодефицитной анемии и анемии хронического заболевания соответственно, а также ответа на эритропоэз-стимулирующую терапию [9, 10]. Причем оба этих параметра: уровень растворимых рецепторов и ферритиновый индекс у пациентов с ХБП продемонстрировали большую чувствительность, чем ферритин и насыщение трансферрина [9, 11].
Таким образом, целью нашего исследования было изучение особенностей феррокинетики у диализных пациентов с учетом уровня растворимых рецепторов трансферрина и ферритинового индекса.
ПАЦИЕНТЫ И МЕТОДЫ
В исследование были включены 100 пациентов с ХБП С5д стадии, получающих программный гемодиализ (ГД), средний возраст которых составил 53,4±15,8 года, среди них 51 женщина и 49 мужчин. Всем больным процедуру гемодиализа осуществляли на аппаратах «BBraun Dialogue Plus» (Германия) с использованием бикарбонатной буферной диализной жидкости и полисульфоновых высокопоточных диализных мембран с площадью поверхности от 1,5 до 2,3 м2 в следующем режиме: три раза в неделю по 4,5 ч, при этом диализная доза (Kt/v) соответствовала критериям адекватности и составила 1,41±0,08, продолжительность заместительной почечной терапии 20,1±21,9 мес (минимум 2 и максимум 115 мес).
Пациентам проведены следующие лабораторные исследования: общий анализ крови с подсчетом эритроцитарных индексов, биохимический анализ крови с определением параметров белкового обмена, воспалительных маркеров, показателей феррокинетики, в том числе определение сывороточного уровня гепсидина-25, растворимых рецепторов трансферрина методом количественного ИФА («Luminex MAGPIX», США) и расчет ферритинового индекса по формуле sTfR/lgFer, где sTfR - растворимые рецепторы траснферрина (мг/л), Fer - ферритин (мкг/л).
Статистический анализ выполняли с помощью программ «Microsoft Office Excel 2010» («Microsoft Corp.», США) и «STATISTICA 7.0» («StatSoft Inc.», США). Результаты представлены в виде средняя арифметическая (M) ± стандартное отклонение (SD). При нормальном распределении выборки для сравнения средних величин использовали критерий Стьюдента, а при отличии от нормального - критерий Манна-Уитни. Корреляционный анализ при нормальном распределении выборки осуществляли с помощью коэффициента Пирсона, при несимметричном - коэффициента Спирмена. Проверку на нормальность распределения проводили с помощью критерия Колмогорова-Смирнова и Шапиро-Уилка. Нулевую статистическую гипотезу об отсутствии различий и связей отвергали при p<0,05.
РЕЗУЛЬТАТЫ
Повышение концентрации растворимых рецепторов трансферрина наблюдалось у 44% пациентов, что может быть обусловлено дефицитом железа и усилением эритропоэза в ответ на терапию эритропоэтинами. Уровень растворимых рецепторов трансферрина статистически значимо не варьировал в группах пациентов в зависимости от степени тяжести анемии и достижения целевого уровня гемоглобина (табл. 1).
При оценке типа нарушений обмена железа применено два подхода: первый - в соответствии с рекомендациями KDIGO (2012) [12], второй - в зависимости от ферритинового индекса. Исходя из рекомендаций KDIGO (2012) по уровню фер- ритина и насыщению трансферрина, абсолютный дефицит железа был выявлен у 28 % пациентов, функциональный - у 9%, дефицит железа не определялся у 63% больных, причем в представленных группах отмечена вариабельность ряда показателей феррокинетики (табл. 2).
Таблица 1
Показатели обмена железа в группах пациентов с анемией различной степени тяжести и в зависимости от достижения целевого уровня гемоглобина
|
Показатель |
Степень тяжести анемии |
|||||
|---|---|---|---|---|---|---|
|
Нормальный уровень гемоглобина |
Гемоглобин более 90 г/л, но менее нормы |
Гемоглобин 70-90 г/л |
Гемоглобин менее 70 г/л |
|||
|
Растворимые рецепторы транс- феррина, нмоль/л (n=80) |
37±10,7 (n=8) |
37,9±13,1 (n=48) |
38,6±13,3 (n=18) |
29,1±8,5 (n=6) |
||
|
Достижение целевого уровня гемоглобина |
||||||
|
Гемоглобин менее 100 г/л |
Гемоглобин 100-120 г/л |
Гемоглобин боле 120 г/л |
||||
|
Растворимые рецепторы трансферрина, нмоль/л (n=80) |
35,2±12,4 (n=34) |
38,8±13,7 (n=33) |
39,1±10,3 (n=13) |
|||
Таблица 2
Показатели феррокинетики у пациентов с дефицитом железа и без него

* Н-тест=20,3, р<0,0001, χ2=13,9, р=0,001; ** р>0,05 (дисперсионный анализ ANOVA).
Ферритиновый индекс, соответствующий анемии хронического заболевания (<1), был выявлен у 92,5% пациентов (0,57±0,17, n=74), характерный для сочетания анемии хронического заболевания и железодефицитной анемии (1-2) - у 7,5% пациентов (1,14±0,11, n=6). Ферритиновый индекс, превышающий 2, не был выявлен ни у одного пациента, что говорит об отсутствии у обследованных больных изолированной железодефицитной анемии. Изменения показателей обмена железа в зависимости от значения ферритинового индекса статистически не различались и представлены в табл. 3.
Недостаточность питания играет важную роль в формирование анемии, что также необходимо учитывать в отношении феррокинетики. В ходе исследования установлена достоверная разница в значениях ряда показателей обмена железа и концентрации альбумина в соответствии с критериями K. Kalantar-Zadeh и соавт. (2001) [13] (табл. 4).
Оценка системного воспаления проводилась с учетом уровня С-реактивного белка (СРБ), причем у 57% пациентов данный показатель превышал референсные значения. Однако статистически значимых различий по показателям феррокинетики у пациентов с нормальным и повышенным уровнем СРБ отмечено не было.
ОБСУЖДЕНИЕ
Исходя из полученных результатов, представляет интерес то обстоятельство, что оценка характера анемии с учетом ферритинового индекса свидетельствует о более высокой распространенности именно функционального дефицита железа, отсутствии пациентов с изолированным (абсолютным) дефицитом микронутриента. При этом сочетание АХЗ с железодефицитом сопряжено с более низкой концентрацией железа и высоким уровнем гепсидина, что свидетельствует в пользу роли гепсидина как отрицательного регулятора обмена железа, обусловливающего формирование анемии при ХБП [14, 15].
Таблица 3
Показатели обмена железа в зависимости от ферритинового индекса
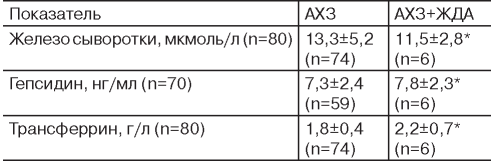
* р<0,05 (дисперсионный анализ ANOVA), АХЗ - анемия хронического заболевания, ЖДА - железодефицитная анемия.
Таблица 4
Изменения показателей феррокинетики в зависимости от уровня альбумина
|
Показатель |
Альбумин |
|
|---|---|---|
|
<35 г/л |
>35 г/л |
|
|
Железо, мкмоль/л (р=0,001) |
8,6±2,6 |
13,4±5,2 |
|
Насыщение трансферрина, % |
19,9±6,7 |
30,6±12,0* |
|
Растворимые рецепторы транс- феррина, нмоль/л |
28,1±13,1 |
38,2±12,3* |
|
Ферритиновый индекс (р=0,04) |
0,47±0,23 |
0,63±0,22 |
*р<0,05.
Более чем у половины пациентов установлено наличие системного воспаления по уровню СРБ, однако, ассоциации значения СРБ и показателей феррокинетики в исследовании выявлено не было, что не соотносится с литературными данными, свидетельствующими в пользу отрицательной роли воспаления в процессе формирования дефицита железа [16]. Подобные особенности, вероятно, обусловлены тем обстоятельством, что СРБ является важным, но не единственным маркером воспаления. Наличие гипоальбуминемии ассоциировано у пациентов с ХБП с дефицитом железа сыворотки, низким значением насыщения трансферрина и растворимых рецепторов трансферрина, что обусловлено негативным влиянием синдрома мальнутриции на активность эритропоэза [17].
ЗАКЛЮЧЕНИЕ
У диализных пациентов для комплексной оценки обмена железа целесообразно выполнять исследование растворимых рецепторов трансферрина и расчет ферритинового индекса, которые позволяют уточнить патогенетические механизмы формирования анемического синдрома.
Источник финансирования. Работа выполнена при поддержке Федерального государственного бюджетного учреждения «Фонд содействия развитию малых форм предприятий в научно-технической сфере» (грант 0007957).
Список литературы
1. Смирнов АВ, Шилов ЕМ, Добронравов ВАидр. Национальные рекомендации. хроническая болезнь почек: основные принципы скрининга, диагностики, профилактики и подходы к лечению. Нефрология 2012; 16(1): 89-115
2. Смирнов АВ, Румянцев АШ, Добронравов ВА, Каюков ИГ. XXI век - время интегративной нефрологии Нефрология 2015; 19 (2): 22-26
3. Coresh J, Astor BC, Greene T et al. Prevalence of chronic kidney disease and decrease kidney function in adult. Am J Kidney Dis 2003; 41 (91): 1-12
4. Mc Clellan W, Aronoff SL, Bolton WK et al. The prevalence of anemia in patients with chronic kidney disease. Curr Med Ress Opion. 2004; 20: 1501-1510
5. Милованов ЮС, Милованова ЛЮ, Козловская ЛВ. Нефрогенная анемия: патогенез, прогностическое значение, принципы лечения. Клин нефрология 2010; 6: 7-18
6. Лапина ЕС, Батюшин ММ, Гуржиева КСидр. Метаболизм железа и гепсидина у пациентов с хронической болезнью почек С5Д стадии. Нефрология 2015; 5 (19): 81-85
7. Feelders RA, Kuiper-Kramer EPA, Henk G van Eijk. Structure, Function and Clinical Significance of Transferrin Receptors. Clinical Chemistry and Laboratory Medicine 2005; 37 (1): 1-10
8. Speeckaert MM, Speeckaert R, Delanghe JR. Biological and clinical spects of soluble transferrin receptor. Crit Rev Clin Lab Sci 2010 Dec; 47(5-6): 213-28. doi: 10.3109/10408363.2010.550461
9. Tarng DC, Huang TP. Determinants of circulating soluble transferrin receptor level in chronic haemodialysis patients. Nephrol Dial Transplant 2002 Jun; 17(6): 1063-1069
10. Castel R, Tax MG, Droogendijk J et al. The transferrin/ log(ferritin) ratio: a new tool for the diagnosis of iron deficiency anemia. Clin Chem Lab Med 2012; 50(8): 1343-9. doi: 10.1515/ cclm-2011-0594
11. Chen YC, Hung SC, Tarng DC. Association Between Transferrin Receptor-Ferritin Index and Conventional Measures of Iron Responsiveness in Hemodialysis Patients. Am J Kid Dis 2006; 47 (6): 1036-1044
12. Клинические практические рекомендации KDIGO по анемии при хронической болезни почек 2012 URL: http://www. kdigo.org/clinical_practice_guidelines/pdf/Anemia%20GL%20 %20Full%20Russian%20Translation.pdf (дата обращения: 13.01.2016)
13. Kalantar-Zadeh K, Kopple JD, Block G et al. A malnutritioninflammation score is correlated with morbidity and mortality in maintenance hemodialysis patients. Am J Kidney Dis 2001; 38 (6): 1251-1263
14. Rishi G, Wallace DF, Subramaniam VN. Hepcidin: regulation of the master iron regulator. Biosci Rep 2015; 35(3). pii: e00192. doi: 10.1042/BSR20150014
15. Lukaszyk E, Lukaszyk M, Koc-Zorawska E et al. Iron Status and Inflammation in Early Stages of Chronic Kidney Disease. Kidney Blood Press Res 2015; 40(4): 366-373. doi: 10.1159/000368512.
16. Garibotto G, Sofia A, Saffioti S et al. Amino acid and protein metabolism in the human kidney and in patients with chronic kidney disease. Clin Nutr 2010 Aug; 29(4): 424-33. doi: 10.1016/j. clnu.2010.02.005
Об авторах
Е. С. ЛапинаРоссия
М. М. Батюшин
Россия
Рецензия
Для цитирования:
Лапина Е.С., Батюшин М.М. Растворимые рецепторы трансферрина и ферритиновый индекс в оценке метаболизма железа у диализных пациентов. Нефрология. 2016;20(5):50-54.
For citation:
Lapina E.S., Batiushin M.M. Soluble transferrin receptor and ferritin index in evaluation of iron metabolism in hemodialysis patients. Nephrology (Saint-Petersburg). 2016;20(5):50-54. (In Russ.)








































