Перейти к:
Особенности кардиоренального континуума у пациентов с метаболическим синдромом
Аннотация
Для цитирования:
Румянцев А.Ш., Шишкин А.Н., Минкин С.Р., Шевелева М.А. Особенности кардиоренального континуума у пациентов с метаболическим синдромом. Нефрология. 2016;20(5):75-83.
For citation:
Rumyantsev A.Sh., Shishkin A.N., Minkin S.R., Sheveleva M.A. Features of cardiorenal relationships in patients with metabolic syndrome. Nephrology (Saint-Petersburg). 2016;20(5):75-83. (In Russ.)
ВВЕДЕНИЕ
По данным ВОЗ, распространенность сердечнососудистых заболеваний составляет около 30%, обуславливая 17,5 млн смертей ежегодно [1]. Взаимосвязь дисфункции почек с неблагоприятным сердечно-сосудистым прогнозом давно привлекает внимание нефрологов. Она обусловлена сходством многофакторной этиологии и патогенетических механизмов развития хронической болезни почек (ХБП) кардиоваскулярной патологии, таких как дисфункция эндотелия, активация ренин-ангиотензин-альдостероновой системы, оксидативный стресс, системный воспалительный ответ. В результате возникает параллелизм между формированием и прогрессированием атеросклероза и гломеруло склероза с повышением риска развития сердечно-сосудистых и почечных осложнений. Однако ведущие специалисты в области кардиологии и нефрологии по-разному подходят к описанию взаимосвязей между сердечнососудистыми заболеваниями и дисфункцией почек, определяя их как либо кардиоренальный (ренокардиальный) синдром [2-4], либо как кардиоренальный континуум [5, 6].
У пациентов с сочетанием ХБП и сердечнососудистой патологией те или иные метаболические нарушения выявляют всегда. Вместе с тем, известен термин «метаболический синдром» (МС), к критериям которого не относят дисфункцию почек, несмотря на то, что последние принимают активное участие во всех видах обмена веществ. Хорошо известны, как минимум, 5 определений МС: ВОЗ [7], Национальной образовательной программы по холестерину [8], Европейской группы по изучению инсулинорезистентности [9], Американской ассоциации клинических эндокринологов [10], Международной федерации диабета [11]. Целью данной статьи не является подробный сравнительный анализ перечисленных рекомендаций. Мы придерживаемся позиции отечественных кардиологов [12].
Вопрос о том, следует ли в ситуации, при которой имеется сочетание сердечно-сосудистого заболевания, ХБП и МС говорить об отдельном синдроме, не может подробно рассматриваться в оригинальной статье. Однако термина, который объединял бы перечисленные и часто сочетающиеся патологические состояния, не предложено. В связи с этим подходы к диагностике, лечению и профилактике в известной степени могут различаться в зависимости от того, какого специалиста посещает больной: кардиолога, нефролога или эндокринолога. На наш взгляд любой пациент требует интегративного подхода, независимо от того, какое заболевание было диагностировано в первую очередь [13].
Целью нашего исследования было изучение кардиоренальных взаимоотношений у больных с МС.
ПАЦИЕНТЫ И МЕТОДЫ
Ретроспективное поперечное когортное исследование проводилось на базе СПбГБУЗ «Елизаветинская больница» в октябре 2015 г. - январе 2016 г. Были изучены истории болезни 100 пациентов кардиологического профиля, из них 45 мужчин и 55 женщин, средний возраст которых составил 58,5±10,4 года. У 95 человек диагностирована ИБС, у 98 - гипертоническая болезнь (ГБ), у 48 - имелись признаки МС, у 46 - кардиоренального синдрома 2-го типа (КРС2).
Пациентов распределили на 4 группы. В 1-ю группу были включены 35 пациентов без МС и КРС2 (группа контроля). Мы не являемся единомышленниками концепции C.Ronco [14], поэтому предпочитаем говорить не о кардиоренальном синдроме, а о кардиоренальных взаимоотношениях и используем первый термин только для удобства изложения и отдавая дань уважения талантливому ученому. 2-ю группу составили 17 пациентов с КРС2, у которых отмечалось снижение СКФ менее 60 мл/мин/1,73 м2 или наличие альбуминурии/про- теинурии. В 3-ю группу вошли 19 пациентов с МС. Мы использовали критерии МС в соответствии с рекомендациями экспертов Всероссийского научного общества кардиологов по диагностике и лечению метаболического синдрома [7]. Критериями МС считали нарушение углеводного обмена в виде нарушения толерантности к углеводам по результатам перорального глюкозотолерантного теста [15], дислипидемию (концентрацию в сыворотке крови ЛПВП менее 1,0 ммоль/л у мужчин и менее 1,2 ммоль/л у женщин, триглицеридов более 1,7 ммоль/л, общего холестерина более 5,2 ммоль/л или/и ЛПНП более 3,3 ммоль/л), избыточную масса тела (ИМТ >25 кг/м2) или ожирение (ИМТ >30 кг/м2) и величину артериального давления более 130/85 мм рт. ст. В 4-ю группу были включены 29 пациентов с КРС2 и МС.
У всех больных, помимо выполнения традиционных рутинных лабораторных и инструментальных методов исследования, рассчитывали скорость клубочковой фильтрации по формуле CKDEPI [16]. Также выполняли эхокардиографическое исследование в обычном и стрессовом режимах в сопоставлении с результатами коронарной ангиографии. Рассчитывали индекс коморбидности CIRS (Cumulative Illness Rating Scale) [17].
Статистический анализ данных производили с использованием пакета прикладных статистических программ «STATISTICA v.10» (StatSoft Inc», США). Результаты представлены при нормальном распределении в виде среднего арифметического ± стандартное отклонение М±SD), при асимметричном - в виде медианы и интерквартильного размаха (Ме, 25 квартиль-75 квартиль). Проверку нормальности распределения осуществляли с использованием критерия Шапиро-Уилка. Для сравнения количественных показателей использовали U-тест Манна-Уитни или t-критерий Стьюдента. Для сравнения качественных показателей применяли точный критерий Фишера. Оценку силы связи между количественными признаками проводили с помощью рангового коэффициента корреляции (Rs) Спирмена или коэффициента корреляции (г) Пирсона. Возрастную скорость снижения СКФ определяли по результатам линейного регрессионного анализа. Для вычисления отношения шансов использовали логистический регрессионный анализ. Нулевую статистическую гипотезу об отсутствии различий и связей отвергали при p<0,05.
РЕЗУЛЬТАТЫ
В табл. 1 приведены основные клиниколабораторные данные о группах обследованных пациентов. При нормальной форме показатели представлены как среднее арифметическое ± стандартное отклонение (нормальное распределение), при отклонении от нормальнй в форме медиана (нижний-верхний квартили).
Таблица 1
Основные клинико-лабораторные данные в группах обследованных пациентов
Показатель | Группа 1 n=35 | Группа 2 n=17 | Группа 3 n=19 | Группа 4 n=29 | р |
|---|---|---|---|---|---|
1 | 2 | 3 | 4 |
| |
Возраст, лет | 55,5±9,5 | 60,2±10,8 | 56,1±10,2 | 60,4±10,5 |
|
Пол, М/Ж | 18/19 | 8/9 | 9/9 | 12/18 |
|
ИМТ, кг/м2 | 24,3±3,3 | 24,6±2,7 | 30,5±4,5 | 31,9±5,4 | 1/3=0,0001 1/4=0,0001 2/3=0,0001 2/4=0,0001 |
CIRS, баллы | 9,0 (7,0±12,0) | 8,0 (6,0-10,0) | 8,5 (6,0-13,0) | 10,0 (9,0-14,0) | 1/4=0,024 2/4=0,006 |
Т ССС, лет | 7,0 (3,0-10,0) | 8 (5-15) | 10 (3-12) | 11 (5-15) | 1/4 =0,021 |
САД, мм рт. ст. | 140 (130-160) | 140 (130-150) | 142 (130-150) | 140 (130-160) |
|
ДАД, мм рт. ст. | 85 (80-90) | 85 (80-90) | 87,5 (80-90) | 86,5 (80-90) |
|
Эритроциты, х109/л | 4,59±0,34 | 4,44±0,57 | 4,65±0,49 | 4,59±0,47 |
|
Гемоглобин, г/л | 140,8±13,0 | 132,4±18,0 | 140,1±12,0 | 134,7±15,7 |
|
СОЭ, мм/ч | 14,0 (9,0-21,0) | 12,0 (10,0-20,0) | 13,5 (8,0-16,0) | 22,0 (8,0-36,0) | 1/4 =0,021 3/4 =0,007 |
С-реактивный белок, г/л | 2,6 (1,3-5,1) | 3,5 (1,4-8,9) | 2,5 (1,2-4,8) | 4,6(2,8-6,4) |
|
Креатинин, мкмоль/л | 78,0 (71,0-87,0) | 92,0 (76,0-96,0) | 79,0 (54,0-98,0) | 100,0 (91,0-118,0) |
|
Мочевина, ммоль/л | 4,4 (3,7-5,5) | 5,3 (4,9-7,2) | 4,4 (3,3-5,7) | 6,5 (5,3-9,8) | 1/2=0,014 2/3=0,036 1/4 =0,0001 3/4=0,0002 |
СКФ, мл/мин/1,73м2 | 84,3±17,1 | 72,2±20,0 | 85,2±15,2 | 60,7±19,6 | 1/4 =0,0001 1/2 =0,041 2/3=0,041 3/4=0,0001 |
Глюкоза ммоль/л | 5,5±1,4 | 5,7±1,5 | 7,8±2,8 | 7,9±3,7 | 1/3=0,0001 2/3=0,0001 1/4=0,0001 2/4=0,0001 |
ОХ, ммоль/л | 4,9 (4,3-6,7) | 4,5 (4,0-5,7) | 6,2 (4,3-7,7) | 6,2 (5,8-7,1) | 1/4 =0,019 2/4=0,013 |
ЛПНП, ммоль/л | 3,0 (2,0-3,9) | 2,8 (2,0-3,8) | 3,5 (2,4-4,0) | 3,6 (3,0-4,1) | 1/4 =0,027 2/4=0,043 |
ЛПВП, ммоль/л | 1,3 (1,2-1,4) | 1,2 (1,1-1,3) | 1,2 (1,1-1,3) | 1,2 (1,1-1,3) |
|
ТГ, ммоль/л | 1,5 (1,1-2,1) | 2,0 (1,6-2,6) | 1,8 (1,1-2,8) | 2,3 (1,5-3,2) | 1/2 =0,045 1/4 =0,005 |
КДО ЛЖ, мл | 93,1±14,8 | 98,8±14,2 | 98,8±15,5 | 100,5±14,7 | 1/4 =0,049 |
ФВ, % | 65,0 (61,0-67,0) | 64,0 (60,0-69,0) | 63,5 (59,0-68,0) | 64,0 (58,0-66,0) |
|
ИММЛЖ, г/м2 | 82,0 (78,0-89,0) | 86,0 (81,0-87,0) | 92,0 (84,0-96,0) | 98,0 (84,0-96,0) | 1/3=0,023 1/4 =0,0001 |
E/A | 1,56 (1,52-1,60) | 1,55 (1,52-1,59) | 1,56 (1,55-1,58) | 1,53 (1,52-1,56) |
|
IVRT, мс | 72,0 (69,0-75,0) | 72,0 (71,0-74,0) | 72,0 (70,0-74,0) | 73,5 (72,0-75,0) |
|
DT, мс | 175,0 (160,0-193,0) | 176,0 (168,-187,0) | 176,5 (171,0-183,0) | 181,5 (173,0-187,0) |
|
Примечание. ИМТ - индекс массы тела, CIRS - баллы по шкале коморбидности, Т ССС - длительность основного заболевания, САД - систолическое артериальное давление, ДАД - диастолическое артериальное давление, ОХ - общий холестерин, ЛПНП - липопротеиды низкой плотности, ЛПВП - липопротеиды высокой плотности, ТГ - триглицериды, ФВ - фракция выброса, ИММЛЖ - индекс массы миокарда левого желудочка, КДО ЛЖ - конечное диастолическое давление в левом желудочке, Е/А - отношение пика Е к пику А, IVRT - время изоволюмического расслабления левого желудочка, DT - время замедления раннего диастолического наполнения левого желудочка.
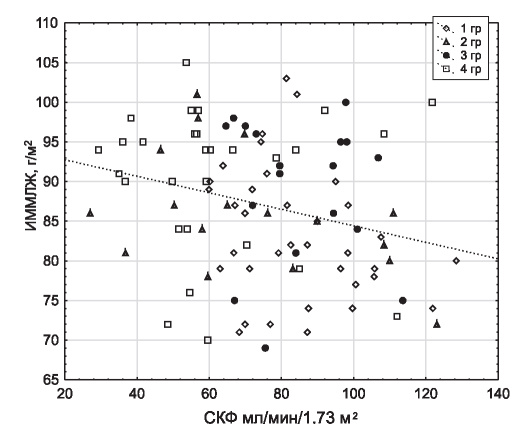
Рис. 1. Взаимосвязь между СКФ и ИММЛЖ.
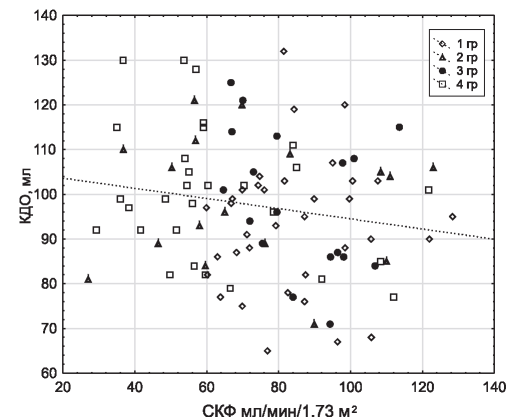
Рис. 2. Взаимосвязь между величиной СКФ и КДО.
По полу и возрасту статистически значимых различий между группами выявлено не было. У пациентов 3-й и 4-й групп средний ИМТ соответствовал ожирению I степени. Среднее количество баллов по шкале CIRS во всех группах свидетельствовало о коморбидности легкой степени. Вместе с тем, у 70% пациентов в 4-й группе количество баллов превышало 10. Наиболее высокая длительность основного заболевания сердечнососудистой системы также отмечалась у пациентов 4-й группы. Среднее АД между группами не различалось и колебалось в пределах от высокого нормального до артериальной гипертензии I степени. Показатели эритроцитов и гемоглобина были нормальными. Средняя величина СОЭ достигала 22 мм/ч в 4-й группе, при этом, уровень С-реактивного белка не превышал референтных значений. Количество пациентов с величиной СКФ менее 60 мл/мин/1,73 м2 в 4-й группе было в 1,5 раза больше по сравнению со 2-й. Средняя концентрация глюкозы в сыворотке крови превышала нормальные значения в 3-й и 4-й группах. В 1-й группе средние показатели липидограммы соответствовали целевым значениям. Вместе с тем, у больных с МС лишь концентрация ЛПВП была нормальной, а наиболее выраженные нарушения липидного обмена отмечались у пациентов 4-й группы (тип IIb по Фредриксону). Величина фракции выброса и показателей диастолической функции левого желудочка были нормальными у всех обследуемых. Величина индекса массы миокарда левого желудочка и конечного диастолического объема были нормальными, однако, наиболее высокие их значения отмечались в 4-й группе.
Таким образом, несмотря на то, что средняя длительность основного заболевания у пациентов всех групп колебалась от 7 до 11 лет, его течение можно охарактеризовать как относительно стабильное.
При проведении непараметрического корреляционного анализа были выявлены взаимосвязи, представленные на рис. 1-3. На рис. 1 показана ассоциация между СКФ и индексом массы миокарда левого желудочка (ИММЛЖ) (Rs=-0,266; р=0,008). Следует отметить, что ни у одного из пациентов величина ИММЛЖ не достигала значений, характерных для гипертрофии левого желудочка. Вместе с тем, прослеживалась отчетливая тенденция к увеличению показателя по мере снижения СКФ. В наибольшей мере это касалось больных 4-й группы.
На рис. 2 представлена негативная взаимосвязь между величиной СКФ и конечным диастолическим объемом (КДО) (Rs =-0,198; р=0,047). Величина КДО у всех пациентов не превышала нормальных значений. Тем не менее, прослеживалась отчетливая тенденция к увеличению показателя по мере снижения СКФ. В наибольшей мере это также касалось больных 4-й группы.
В табл. 2 приведены результаты регрессионного анализа между СКФ и возрастом.
Учитывая величину коэффициентов регрессии, можно судить о том, что при увеличении возраста на 1 год СКФ снижалась в 1-й группе на 0,8 мл/1,73 м2/год, во 2-й группе - на 1,5 мл/1,73 м2/ год, в 4-й группе - на 1,4 мл/1,73 м2/год. Для 3-й группы статистически значимой модели получено не было. Следовательно скорость прогрессирования ХБП у пациентов с КРС2 и сочетанием КРС2 с МС практически одинакова и почти в 2 раза превышает таковую у больных с патологией сердечно-сосудистой системы без повреждения почек.
Таблица 2
Результаты регрессионного анализа между СКФ и возрастом
Показатель | Стандартизированный коэффициент регрессии β | Стандартная ошибка β | Коэффициент регрессии В | Стандартная ошибка В | р |
|---|---|---|---|---|---|
1-я группа: n=35, R2=0,238, F=10,310, p=0,002 | |||||
Свободный член |
|
| 133,256 | 15,442 | 0,0001 |
Возраст | -0,487 | 0,151 | -0,880 | 0,274 | 0,002 |
2-я группа: n=17, R2=0,365, F=8,625, p=0,010 | |||||
Свободный член |
|
| 166,121 | 32,451 | 0,0001 |
Возраст | -0,604 | 0,205 | -1,558 | 0,530 | 0,0102 |
3-я группа: n=19, | R2=0,0001, F=0,003, p=0,956 |
|
|
|
|
Свободный член |
|
| 86,393 | 21,265 | 0,0009 |
Возраст | -0,013847 | 0,249 | -0,020 | 0,373 | 0,956 |
4-я группа: n=29, R2=0,363, F=15,968, p=0,0004 | |||||
Свободный член |
|
| 148,890 | 22,348 | 0,0001 |
Возраст | -0,602 | 0,150 | -1,411 | 0,353 | 0,0004 |
Таблица 3
Частота приема кардио/нефропротективных препаратов
Группа препаратов | 1-я группа n=35 | 2-я группа n =17 | 3-я группа n =19 | 4-я группа n =29 | р, точный метод Фишера |
|---|---|---|---|---|---|
ИАПФ, да/нет | 12/23 | 10/7 | 9/10 | 16/13 | 0,286 |
БРА, да/нет | 8/27 | 4/13 | 21/17 | 8/21 | 0,346 |
Блокаторы кальциевых каналов | 3/32 | 2/15 | 4/15 | 6/23 | 0,311 |
β-блокаторы, да/нет | 12/23 | 13/4 | 12/7 | 17/12 | 0,017 |
Статины, да/нет | 5/30 | 7/10 | 5/14 | 6/23 | 0,172 |
Дезагреганты, да/нет | 10/25 | 8/9 | 9/10 | 16/13 | 0,228 |
Примечание. ИАПФ - ингибиторы ангиотензинпревращающего фермента, БРА - блокаторы рецепторов к ангиотензину II (тип I).
В табл. 3 представлена частота приема кардио/ нефропротективных препаратов в группах обследуемых.
ИАПФ получали 34% пациентов в 1-й группе и от 50 до 59% в остальных группах. БРА использовались существенно реже по сравнению с ИАПФ: в 1-й группе - у 29%, во 2-й группе - у 24%, в 3-й группе - у 6% и в 4-й группе - у 27% обследуемых. Блокаторы кальциевых каналов получали в 1-й группе 9%, во 2-й группе - 12%, в 3-й группе - 22%, в 4-й группе - 20%. β-блокаторы применялись во 2-4-й группах у 57-76%, но лишь у 34% больных в 1-й группе. Статины принимали 12% в 1-й, 41% во 2-й, 28% в 3-й группе и 20% в 4-й группе пациентов. Дезагреганты получали 29% в 1-й группе и 47-53% во 2-4-й группах обследуемых.
На рис. 3 представлена негативная ассоциация между величиной СКФ и уровнем ЛПНП среди пациентов, не принимавших статины (Rs=-0,343; p=0,002). Наиболее высокие значения концентрации ЛПНП были отмечены при низких значениях СКФ, главным образом, у больных 4-й группы.
При проведении логистического регрессионного анализа риск развития гемодинамически значимого коронарного стеноза в 4-й группе увеличивался в 3,6 раза по сравнению с 1-й группой.
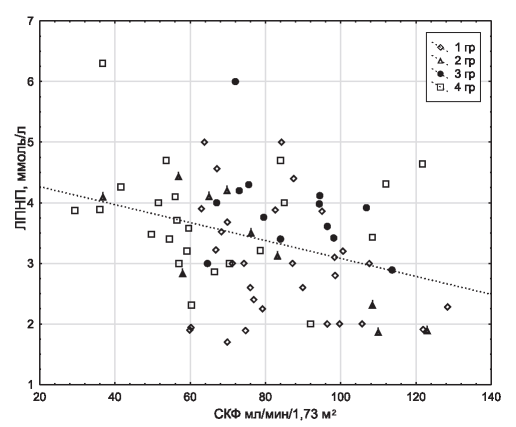
Рис. 3. Взаимосвязь между величиной СКФ и уровнем ЛПНП среди пациентов, не принимавших статины.
Таблица 4
Результаты логистического регрессионного анализа между гемодинамически значимым коронарным стенозом и сочетанием КРС2, МС и ХБП. χ2=4,668, p=0,035
Показатель | Const. B0 | Гемодинамически значимый коронарный стеноз |
|---|---|---|
Коэффициент регресии | -0,076 | 1,280 |
Стандартная ошибка | 0,277 | 0,714 |
χ2 Вальда | 0,076 | 4,214 |
p | 0,781 | 0,039 |
Отношение шансов |
| 3,600 |
-95% ДИ |
| 0,863 |
+95% ДИ |
| 15,007 |
При проведении коронароангиографии показания к стентированию были выявлены у пациентов 1-й группы в 29%, 2-й - в 12%, 3-й - в 17%, 4-й - в 10% случаев (χ2=4,420, р=0,219).
ОБСУЖДЕНИЕ
Конец XX и начало XXI в. ознаменовались интенсивным развитием биологии и медицины, переосмыслением ряда концепций. Одна из трактовок классического закона философии о переходе количества в качество может быть представлена в следующем виде: «Развитие осуществляется путём накопления количественных изменений в предмете, что неизбежно приводит к нарушению его меры (стабильного состояния) и скачкообразному превращению в качественно новый предмет» [18]. Соответственно накопление новых знаний способствовало появлению новых классификаций. В качестве примера можно привести концепцию ХБП [19] и острого повреждения почек [20, 21]. Каждая из них является плодом труда групп узких специалистов, однако создается для использования не только в основной, но и смежных областях медицины. Обе упомянутые концепции с известными трудностями внедрялись в различных странах мира, что подтверждает наличие здорового консерватизма в медицинской среде. Однако, несмотря на то, что они официально приняты, и в настоящее время в ряде учебников для медицинских вузов можно увидеть главы, посвященные хронической и острой почечной недостаточности.
Наряду с новыми концепциями, появляются и новые синдромы. Ряд из них имеют четкие критерии и объективное патогенетическое обоснование. В качестве примеров можно назвать ишемическое прекондиционирование, станнирование и гибернацию миокарда, отражающие адаптацию последнего к ишемии/реперфузии [22, 23]. КРС и МС подобной четкостью не отличаются, что в определенной мере подтверждают полученные нами результаты.
При распределении пациентов мы выделили группу, которую считали контрольной. В нее были включены 35 человек, не имевших признаков повреждения почек и МС. Эти пациенты отличались относительно небольшой длительностью течения ИБС или ГБ с СН I-II ф. кл., нормальной массой тела и отсутствием нарушений толерантности к глюкозе.
Во 2-ю группу включили 17 человек с нормальной массой тела, клиническими проявлениями СН I-II ф. кл. без первичной патологии мочевыделительной системы, отсутствием нарушений толерантности к углеводам, но с признаками ХБП. Клинически они соответствовали представлению о КРС2 [24]. Однако при ЭХО-КГ у больных не выявили признаков систолической или диастолической дисфункции миокарда левого желудочка. По остальным исследуемым показателям статистически значимых различий по сравнению с 1-й группой выявлено не было, кроме более высокой концентрации ТГ в сыворотке крови и снижения уровня СКФ.
В 3-ю группу были отнесены пациенты, соответствовавшие критериям МС, т.е. имевшие избыточную массу тела, признаки нарушения толерантности к глюкозе, артериальную гипертензию и дислипидемию. Клинических проявлений атеросклероза, СН и лабораторных признаков ХБП у этих пациентов выявлено не было. Они отличались от контрольной группы более высоким содержанием глюкозы в сыворотке крови и тенденцией к более высокому сывороточному уровню ТГ и ЛПНП.
В 4-ю группу вошли больные с сочетанием признаком ХБП, МС и СН I-II ф. кл. Они отличались от 1-й группы большей продолжительностью основного заболевания сердечно-сосудистой системы, большей выраженностью дислипидемии и коморбидности.
Признаки нарушений геометрии левого желудочка нередко начинают выявлять уже на ранних стадиях ХБП [25]. В нашем исследовании признаков увеличения полости и/или массы левого желудочка выявлено не было. Вместе с тем, отмечена негативная ассоциация между величиной СКФ и ИММЛЖ, а также КДО. Эти данные позволяют думать о том, что всем пациентам с ХБП С1 стадии необходимо выполнять ЭХО-КГ в динамике. Тенденция к увеличению ИММЛЖ и/или КДО даже в пределах нормальных значений, несомненно, требует пересмотра проводимой кардио/ нефропротективной терапии.
Результаты линейного регрессионного анализа свидетельствуют о том, что наличие ХБП в сочетании с метаболическими нарушениями увеличивает темпы возрастного снижения СКФ в 2 раза даже при условии достижения целевых значений артериального давления. Считается, что снижение СКФ, обусловленное возрастными изменениями, начинается в возрасте около 40 лет и составляет примерно 1 мл/мин/1,73 м2 в год. Следовательно, начиная с этого периода, необходимо обеспечивать регулярный мониторинг СКФ у всех пациентов с заболеваниями сердечно-сосудистой и мочевыделительной систем, а также с избыточной массой тела, нарушением толерантности к углеводам или сахарным диабетом. В настоящее время большинство врачей начинают обращать внимание на снижение СКФ лишь в двух случаях: когда ее величина достигает критической цифры 60 мл/мин/1,73 м2у больных без первичной патологии почек или при скорости снижения СКФ более 5 мл/мин/1,73 м2 в год при наличии ХБП. Собственно тогда и начинается проведение нефро/ кардиопротективной терапии, которая пока еще далека от совершенства. Однако, если мы ратуем за профилактическую направленность медицины, стоит обращать внимание на минимальную отрицательную динамику выделительной функции почек, как это уже сделано в отношении критериев определения I стадии острого повреждения почек. Уверены, что при таком подходе можно будет существенно увеличить результативность органосберегающих мероприятий.
На примере нашего небольшого исследования очевидно, что больные получают недостаточное лечение. Мы не ставили своей задачей выяснять, с чем это связано: с медицинскими, социальными факторами, особенностями больного или врача, либо с чем-то другим. Приверженность к лечению невысока во всех странах мира. Несмотря на то, что антигипертензивные препараты являются одним из обязательных компонентов кардио/нефропротекции, в РФ их регулярный прием осуществляют не более 30% лиц, знающих о своем заболевании и целевых цифрах АД [26]. Пациенты 1-й группы принимали препараты, снижающие АД не более, чем в 34% случаев. Преимущество имели ИАПФ и β-блокаторы. Статины использовали лишь 12% пациентов. Как уже говорилось выше, на момент проведения обследования данную группу больных мы считали наиболее благополучной. Конечно, препараты, влияющие на центральную и внутрипочечную гемодинамику, обладают плейотропными свойствами. Однако эти эффекты и носят такое название потому, что их результаты проявляются лишь при условии регулярного приема и в целом не столь значительны. Учитывая то обстоятельство, что, несмотря на имеющиеся показания, статины принимал лишь каждый десятый пациент, можно с высокой долей вероятности предположить, что в перспективе эти больные обречены на ухудшение функции эндотелия, а следовательно, имеют высокий риск как развития сердечно-сосудистых осложнений, так и снижения СКФ.
1-я группа была представлена пациентами с сочетанием заболевания сердечно-сосудистой системы и ХБП, что предполагало необходимость применения у каждого из них активной кардио/ нефропротективной терапии. Однако и в этой группе более чем в 40% никакой вторичной профилактики не проводилось. Неудивительно, что при этом возрастная скорость снижения СКФ была в 1,5 раза выше по сравнению с 1-й группой.
2-я группа включала пациентов с МС. Эти больные имели большую выраженность таких факторов риска сердечно-сосудистых заболеваний и ХБП, как ожирение и нарушение толерантности к углеводам. В связи с этим они должны были получать более активную терапию, направленную на нормализацию массы тела и суточного профиля глюкозы в сыворотке крови, а также устранение дислипидемии. 60% лиц в данной группе имели лишь избыточную массу тела, но не ожирение. Однако с большинством из них никогда не проводилось разъяснительных бесед о практических шагах по снижению массы тела. А больные, принимавшие лекарственные препараты, считали, что они уже достаточно защищены фармакологически и дополнительные мероприятия не требуются. В этой группе нам не удалось получить статистически значимую модель взаимосвязи возраста и скорости снижения СКФ, вероятно, в связи с тем, что влияние возраста на прогрессирование ХБП нивелировалось метаболическими причинами.
3-я группа пациентов отличалась большей выраженностью основных негемодинамических факторов риска прогрессирования основного заболевания и ХБП. Возрастная скорость снижения СКФ была в 1,5 выше по сравнению с контрольной группой. Однако, у этих пациентов характер и агрессивность кардио/нефропротективной терапии практически не отличались от таковой во
4-й и 3-й группах. При этом именно у больных данной группы необходимость хирургического лечения коронарного атеросклероза возрастала в 3,6 раза.
ЗАКЛЮЧЕНИЕ
По данным исследования ЭССЭ-РФ (Эпидемиология сердечно-сосудистых заболеваний и их факторов риска в регионах Российской Федерации), распространенность факторов риска ССЗ составляет: повышенное АД - 33,8%, ожирение - 29,7%, повышенный уровень общего холестерина - 57,6%, повышенный уровень глюкозы в крови/диабет - 4,6%, потребление табака (курение) - 25,7%, недостаточный (низкий) уровень физической активности - 38,8%, избыточное потребление соли - 49,9% недостаточное потребление овощей и фруктов - 41,9% [27]. Мы полагаем, что наличие факторов риска ассоциируется с развитием первичного заболевания - сердечно-сосудистой системы или почек. В дальнейшем недостаточная терапия и отсутствие изменения образа жизни в гораздо большей степени, нежели какие-либо другие причины, способствуют присоединению второй, патогенетически взаимосвязанной с первой, патологии. Если наши рассуждения верны, то как кардиоренальный (ренокардиальный), так и метаболический синдромы являются результатом недостаточного лечения пациента, но не отдельной нозологией. В таком случае основное внимание должно быть обращено не только на разработку новых лекарственных препаратов и оптимизацию схем их применения, но, в первую очередь, на улучшение приверженности больных к лечению [28]. Одним из направлений реализации данной идеи является расширение сети школ для пациентов на уровне амбулаторного звена медицинской помощи. В идеале они могли бы быть организованы в рамках центров здоровья. Как известно: «Истина - дочь времени». Дополнительные исследования в предложенном направлении могут оказаться весьма перспективными не только в плане улучшения прогноза у отдельного взятого пациента, но и в отношении макроэкономических показателей в здравоохранении в целом.
Список литературы
1. Mendis Sh, Puska P, Norrving B. Global atlas on cardiovascular disease prevention and control. Policies, strategies and interventions 2011: 164
2. Шутов АМ, Серов ВА. Кардиоренальный и ренокардиальные синдромы. Нефрология 2009; 13 (4): 63-68
3. Моисеев ВС, Кобалава ЖД. Кардиоренальные синдромы (патогенетические, клинико-диагностические прогностические и терапевтические аспекты). Тер арх 2011; 12:5-11
4. Acute Dialysis Quality Initiative (ADQI) consensus group. Cardio-renal syndromes: report from the consensus conference of the Acute Dialysis Quality Initiative. Europ Heart J (2010) 31, 703-711
5. Смирнов АВ, Добронравов ВА, Каюков ИГ Кардиоренальный континуум: патогенетические основы превентивной нефрологии. Нефрология 2005; 9 (3): 7-15
6. Моисеев ВС, Кобалава ЖД, Ефремовцева МА, Виллевальде СВ. Кардиоренальные взаимоотношения: современные представления. Кардиоваскулярная терапия и профилактика 2010; (4): 4-11
7. Alberti KG1, Zimmet PZ. Definition, diagnosis and classification of diabetes mellitus and its complications. Part 1: diagnosis and classification of diabetes mellitus provisional report of a WHO consultation. Diabet Med 1998 Jul;15(7):539-553
8. Executive Summary of The Third Report of The National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, And Treatment of High Blood Cholesterol In Adults (Adult Treatment Panel III). JAMA 2001 May16;285(19):2486-2497
9. Beck-Nielsen H. General characteristics of the insulin resistance syndrome: prevalence and heritability. European Group for the study of Insulin Resistance (EGIR). Drugs 1999;58 Suppl 1:7-10
10. Einhorn D, Reaven GM, Cobin RH et al. ACE Position Statement on the Insulin Resistance Syndrome. Endocr Pract 2003;9(3):240-252
11. Alberti KGMM, Zimmet P, Shaw J. Metabolic syndrome a new world-wide definition. A consensus statement from the international diabetes federation. Diabet Med 2006; 23:469-480
12. Рекомендации экспертов Всероссийского научного общества кардиологов по диагностике и лечению метаболического синдрома (второй пересмотр). Практическая медицина 2009; 44(5): 81-101)
13. Смирнов АВ, Румянцев АШ, Добронравов ВА, Каюков ИГ. XXI век - время интегративной нефрологии. Нефрология 2015; 19(2): 26-31
14. Ronco C, Di Lullo L. Cardiorenal syndrome. Heart Fail Clin 2014;10(2):251-280
15. Кишкун АА. Руководство по лабораторным методам диагностики. ГЭОТАР-Медиа, М., 2014: 760
16. Stevens LA, Claybon MA, Schmid CH et al. Evaluation of the Chronic Kidney Disease Epidemiology Collaboration equation for estimating the glomerular filtration rate in multiple ethnicities. Kidney Int 2011; 79: 555-562
17. Linn BS, Linn MW, Gurel L. Cumulative illness rating scale. J Amer Geriatr Soc 1968;16: 622-626
18. Петров В. Философия. Курс лекций. Владос, М., 2014: 552
19. Смирнов АВ, Шилов ЕМ, Добронравов ВАидр. Национальные рекомендации. хроническая болезнь почек: основные принципы скрининга, диагностики, профилактики и подходы к лечению. Нефрология 2012; 16(1): 89-115
20. Смирнов АВ, Добронравов ВА, Румянцев АШидр. Национальные рекомендации. Острое повреждение почек: основные принципы диагностики, профилактики и терапии. Часть I. Нефрология 2016; 0(1): 104-108
21. Смирнов АВ, Добронравов ВА, Румянцев АШидр. Национальные рекомендации. Острое повреждение почек: основные принципы диагностики, профилактики и терапии. Часть II. Нефрология 2016; 0(1): 100-105
22. Мареев ВЮ, Агеев ФТ, Арутюнов ГП, Ревишвили АШ. Национальные рекомендации ВНОК и ОССН по диагностике и лечению ХСН (третий пересмотр). Журн сердечн недост 2010;(1): 3-62
23. Canty JM Jr, Suzuki G. Myocardial perfusion and contraction in acute ischemia and chronic ischemic heart disease. J Mol Cell Cardiol 2012;52(4):822-831
24. Cruz DN, Schmidt-Ott KM, Vescovo G et al. Pathophysiology of cardiorenal syndrome type 2 in stable chronic heart failure: workgroup statements from the eleventh consensus conference of the Acute Dialysis Quality Initiative (ADQI). Contrib Nephrol 2013;182:117-136
25. Di Lullo L, Gorini A, Russo D et al. Left Ventricular Hypertrophy in Chronic Kidney Disease Patients: From Pathophysiology to Treatment. Cardiorenal Med 2015;5(4):254-266
26. Агеев ФТ, Смирнова МД, Фофанова ТВ. Повышение приверженности к терапии: «дело техники»? Журн сердечн недост 2011; 12 (4): 238-243
27. Научно-организационный комитет проекта ЭССЭ-РФ. Эпидемиология сердечно-сосудистых заболеваний в различных регионах России (ЭССЭ-РФ. Обоснование и дизайн исследования. Профилактическая медицина 2013; 6:25-34
28. Фофанова ТВ. Приверженность лечению в медицинской практике и возможные методы ее повышения. Кардиол вестн 2011; VI(XVIII), 2:46-53
Об авторах
А. Ш. РумянцевРоссия
А. Н. Шишкин
Россия
С. Р. Минкин
Россия
М. А. Шевелева
Россия
Рецензия
Для цитирования:
Румянцев А.Ш., Шишкин А.Н., Минкин С.Р., Шевелева М.А. Особенности кардиоренального континуума у пациентов с метаболическим синдромом. Нефрология. 2016;20(5):75-83.
For citation:
Rumyantsev A.Sh., Shishkin A.N., Minkin S.R., Sheveleva M.A. Features of cardiorenal relationships in patients with metabolic syndrome. Nephrology (Saint-Petersburg). 2016;20(5):75-83. (In Russ.)
JATS XML








































