ПЕРЕДОВАЯ СТАТЬЯ
Почка является важнейшим органом водного гомеостаза и экскреции токсических субстанций. Она выполняет несколько важных физиологических функций для обеспечения гомеостаза: удаляет циркулирующие продукты метаболизма, регулирует баланс жидкости в организме и действует как иммунный регулятор, а также модулятор нормального функционирования сердечно-сосудистой системы. В самое последнее время появились и активно развиваются модели почечных заболеваний in vitro с плюрипотентными стволовыми клетками (как стволовыми клетками человеческого эмбриона, так и индуцированными плюрипотентными стволовыми клетками), а также разрабатываются надежные протоколы по получению in vitro клеток, подобных специфичным ренальным, из индуцированных плюрипотентных стволовых клеток пациента. В данном обзоре мы приводим главные открытия в области регенерации почки с основным фокусом на развитие пошаговых протоколов по созданию почечных клеток из человеческих плюрипотентных стволовых клеток и самые последние достижения в области биоинжиниринга почки (т.е. децеллюляризированного почечного остова и биопринтинга). Возможность создания трехмерной структуры, подобной почке, с последующим наполнением ее индуцированными плюрипотентными стволовыми клетками почечного происхождения может открыть новые перспективы для создания функционирующего по требованию почечного трансплантата.
Статья переведена на русский язык и опубликована согласно условиям лицензии Creative Commons. Журнал FEBS J. 2016 Sep;283(18):3303–24. doi: 10.1111/febs.13704. Перевод М.С.Храбровой. Редакция перевода И.И.Трофименко
ОБЗОРЫ И ЛЕКЦИИ
Эндотоксин – облигатный компонент клеточной стенки грамотрицательных бактерий – один из основных этиологических факторов хронического воспаления у больных хронической болезнью почек. Тяжесть эндотоксинемии возрастает по мере прогрессирования почечной недостаточности. Основными источниками эндотоксина являются микробиом толстой кишки, а также биопленки, формируемые бактериями, в системе водоподготовки, венозных катетеров и т.д. Эндотоксин вызывает различные стойкие нарушения гомеостаза: клеточного и гуморального иммунитета, метаболические расстройства и др. Коррекция указанных нарушений представляет собой сложную задачу. Эндотоксинемия у больных хронической болезнью почек значительно ухудшает результаты лечения и рост летальности.
В статье отражены основные причины и механизмы развития отторжения почечного аллотрансплантата, описаны современные представления о формировании иммунологической толерантности.
Современная концепция посттрансплантационного введения больных направлена на редукцию иммуносупрессии, при которой отмечается минимальность побочных действий данных препаратов и не возникает отторжение почечного аллотрансплантата. Одним из методов, способствующих снижению риска отторжения и формированию иммунологической толерантности, является фотоферез. В статье представлен обзор литературных данных по применению фотофереза при трансплантациях солидных органов и приведены механизмы его действия.
ОРИГИНАЛЬНЫЕ СТАТЬИ. КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
ЦЕЛЬ – оценить распространенность и тяжесть минерально-костного обмена у пациентов с хронической болезнью почек (ХБП), перенесших трансплантацию почки. ПАЦИЕНТЫ И МЕТОДЫ. В исследование включены 77 больных (32 мужчины, 45 женщин, медиана возраста 44 года) с ХБП, перенесших трансплантацию трупной почки с 2011 по 2015 г. Сывороточные концентрации электролитов, активности общей щелочной фосфатазы (ЩФ), альбумина, параметров азотистого метаболизма определяли по стандартным методикам, паратиреоидный гормон (ПТГ) и витамин D (25-ОН витамин D) в плазме крови – хемилюминесцентным иммуноанализом на системе ARСHITECT. Проведен перерасчет сывороточной концентрации кальция на сывороточную концентрацию альбумина, скорость клубочковой фильтрации (CКФ) рассчитана по формуле CKD-EPI. РЕЗУЛЬТАТЫ. Гиперкальциемия, гипофосфатемия, гипомагниемия и высокий уровень ПТГ диагностированы у 15,6, 16,9, 16,9 и 87% соответственно. Определялась высокодостоверная разница между содержанием ПТГ в крови у пациентов с нормальной и сниженной функцией почечного трансплантата. Уровень витамина D в крови колебался от 6 до 30 нг/мл (медиана 14), только один пациент имел рекомендуемый диапазон (≥30 нг/мл).Установлена обратная корреляционная зависимость ПТГ с СКФ (r=–0,543, р<0,001) и с сывороточной концентрацией магния (r=–0,241, р=0,04), прямая с активностью общей ЩФ (r=0,280, р=0,015). Не установлено ассоциативной связи между содержанием в крови ПТГ и сывороточными концентрациями фосфора и кальция. Определялась слабая корреляционная связь между сывороточной концентрацией фосфора и СКФ (r=–0,232, р=0,04), между активностью ЩФ и СКФ (r=0,267, р=0,02) и между сывороточной концентрацией магния и СКФ (r=0,230, р=0,05). ЗАКЛЮЧЕНИЕ. К распространенным проявлениям минерально-костных нарушений у реципиентов почечного трансплантата относятся пре и посттрансплантационный гиперпаратиреоз, развитие/прогрессирование которого ассоциируется с гипомагниемией, ухудшением функции почки, а также дефицит витамина D.
ЦЕЛЬ ИССЛЕДОВАНИЯ. Проанализировать гистологические результаты применения метода экстракорпоральной фотохимиотерапии при аллотрансплантации трупной почки. ПАЦИЕНТЫ И МЕТОДЫ. Экстракорпоральная фотохимиотерапия была применена для предупреждения острого отторжения почечного аллотрансплантата в раннем послеоперационном периоде у 20 пациентов. Контрольную группу составили 20 пациентов с парными основной группе трансплантатами без применения данного метода. Пациентам обеих групп проводили протокольную биопсию трансплантата на 30-е и 180-е сутки после трансплантации или при наличии показаний с последующим гистологическим заключением согласно классификации Banff 2007 года. Также приведен клинический случай использования экстракорпоральной фотохимиотерапии в качестве терапии гломерулонефрита трансплантата. РЕЗУЛЬТАТЫ. Установлено, что в основной группе по результатам биопсии ни у одного пациента не выявлено признаков отторжения трансплантата, в то же время у 4 пациентов группы сравнения гистологически подтверждено отторжение пересаженного органа различной степени по Banff 2007, два из которых в результате привели к потере трансплантата. Применение экстракорпоральной фотохимиотерапии в качестве терапии гломерулонефрита трансплантата показало, что метод может быть использован с целью нормализации функции трансплантата и способен остановить процесс развития фокального и сегментарного гломерулосклероза, что подтверждено данными гистологического исследования биоптата до и после проведения процедур. ЗАКЛЮЧЕНИЕ. Экстракорпоральная фотохимиотерапия обладает эффективностью и может быть использована в качестве адьювантной терапии для предупреждения отторжения почечного аллотрансплантата и в качестве терапии возвратного гломерулонефрита трансплантата.
ЦЕЛЬ – оценить эффективность использования комбинации внутривенного человеческого иммуноглобулина (ВВИГ) с плазмаферезом и ритуксимабом для лечения трансплантационной гломерулопатии в поздние сроки после трансплантации почки. ПАЦИЕНТЫ И МЕТОДЫ. В исследование было включено 50 пациентов с морфологически верифицированным диагнозом трансплантационной гломерулопатии, 24 из которых получали лечение плазмаферезом в сочетании с ВВИГ и ритуксимабом. Контрольную группу составили 26 пациентов, не получавших антигуморального лечения. РЕЗУЛЬТАТЫ. На момент постановки диагноза СКФ в исследуемой и контрольной группах не различалась (44,9 Ѓ} 21,3 и 41,2 Ѓ} 14,6 мл/мин, р =0,47), однако последующие темпы снижения функции трансплантата были ниже в группе получавших лечение по сравнению с контролем: –0,47 Ѓ} 0,6 мл/мин/мес и 1,31 Ѓ} 1,6 мл/мин/мес (p = 0,02). 3-летняя выживаемость трансплантатов, таким образом, составила 21,3% и 64,8% у пациентов, получавших лечение (р=0,01). ЗАКЛЮЧЕНИЕ. Наше исследование показало, что трансплантационная гломерулопатия, будучи наиболее частым вариантом хронического гуморального отторжения, характеризуется неблагоприятным прогнозом, который мало зависит от особенностей морфологической картины и активности процесса на момент постановки диагноза. Комплексное лечение, включающее сеансы плазмафереза, внутривенный человеческий иммуноглобулин и ритуксимаб, позволяет замедлить темпы прогрессирования хронического отторжения по крайней мере у части пациентов с хроническим гуморальным отторжением, выявленным в поздние сроки после АТП.
ЦЕЛЬ: оценка влияния плазмафереза, проводимого в непосредственном посттрансплантационном периоде, на 15-летние результаты трансплантации почки. ПАЦИЕНТЫ И МЕТОДЫ. 32 детям, оперированным в 1995–1996 годах, плазмаферез не проводили, эта группа больных названа "до ПА". 32 детям, оперированным в 1996–1997 годах, в непосредственном посттрансплантационном проводили плазмаферез. Группа была названа "ПА". 31 ребёнку, оперированному в 1997–1998 годах, плазмаферез также не проводили, но им интенсифицировали индукционную иммунодепрессию путём введения АТГ, внедрением микроэмульсии циклоспорина и СеллСепта. Эту группу назвали "после ПА". Оценивали выживаемость пациентов и трансплантатов в каждой из групп. РЕЗУЛЬТАТЫ. Наибольшей была актуариальная выживаемость как пациентов, так и трансплантатов в группах "ПА" и "после ПА" по сравнению с другими группами, разница статистически достоверна. ЗАКЛЮЧЕНИЕ. Плазмаферез, выполненный в непосредственном посттрансплантационном периоде может оказывать положительное влияние на отдаленные результаты трансплантации почки у детей.
ЦЕЛЬ ИССЛЕДОВАНИЯ: определить частоту выявления и исходы антительно-опосредованного отторжения (AMR, antibody-mediated rejection) при рутинном морфологическом и иммунологическом мониторировании. ПАЦИЕНТЫ И МЕТОДЫ. В исследование вошли 55 реципиентов аллографта почки (АП) согласно критериям включения: совместимость с донором по группе крови, отрицательный цитотоксический кросс-матч-тест, как минимум, три биопсии АП. Все реципиенты получили стандартную иммуносупрессивную терапию: глюкокортикостероиды, базиликсимаб, ингибиторы кальциневрина, микофенолата мофетил. Пациентам выполняли протокольные биопсии (3, 6, 12 мес и далее ежегодно) и/или по показаниям: отсроченная функция АП, подъем креатинина ≥25%, протеинурия ≥1 г/сут или ее нарастание. Биопсии оценивали согласно критериям Banff 2013. Скрининг донор-специфических антител выполняли иммуноферментным анализом, а мониторинг – с помощью мультиплексного анализа Luminex (xMAP Technology). Терапия AMR включала глюкокортикостероиды, плазмаобмен, внутривенный иммуноглобулин, ритуксимаб, бортезомиб. Утрату функции АП и возврат на диализ учитывали как исход. Прогноз аллотрансплантации (АТП) оценивали на основе анализа выживаемости методом Каплана–Мейера. Медиана периода наблюдения от АТП составила 65 (47; 80) мес. РЕЗУЛЬТАТЫ. Морфологические признаки AMR были выявлены в 13% биопсий (n=390), а критерии AMR Banff 2013 – у 45% реципиентов (n=25) в разные сроки посттрансплантационного периода. Острое AMR (aAMR) регистрировали у 13 реципиентов, а хроническое активное (сAMR) – у 12. Субклиническим течение AMR было в 48% случаев. Персистенцию AMR выявили у 56% больных, а хронификацию – у 77%, несмотря на проводимую терапию. Кумулятивная выживаемость пациентов в общей группе за период наблюдения составила 94,5%, выживаемость АП – 79%. Выживаемость АП при AMR была ниже, чем у больных без AMR (73% и 100%, plog-rank=0,016). Различий в выживаемости АП в группах с аAMR и cAMR, а также с клиническим и субклиническим течением AMR выявлено не было. ЗАКЛЮЧЕНИЕ. AMR может быть распространенной и недооцениваемой клинической проблемой, связанной со снижением сроков функционирования АП и эффективности АТП в целом. Своевременное выявление и лечение этого типа иммунного конфликта требует рутинного проведения иммунологического и морфологического мониторинга.
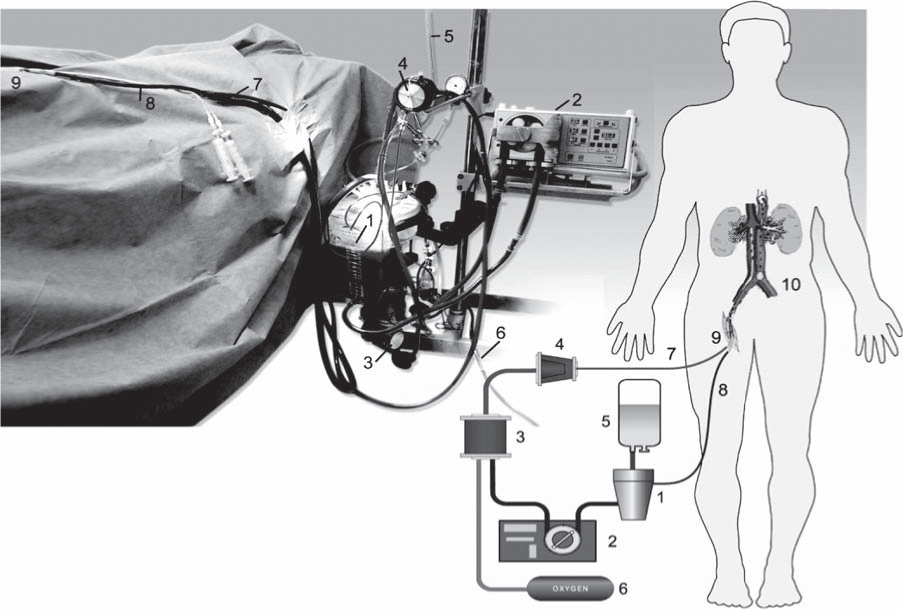
ЦЕЛЬ. Предложить трансплантационному сообществу надежный протокол получения полноценных ренальных трансплантатов от доноров с необратимой остановкой сердца, основанный на оценке 5-летних результаты пересадок почек, полученных с помощью нормотермической перфузии и экстракорпоральной оксигенации. МЕТОДЫ. В исследование были включены 29 АСД почек [время первичной тепловой ишемии – 58,1 (19,39) мин], полученных с использованием предложенного протокола, и оценены результаты пересадок таких трансплантатов у 58 реципиентов. Полученные данные были валидированы путем сравнения с результатами пересадок 112 почек от 115 доноров со смертью мозга (ДСМ). РЕЗУЛЬТАТЫ. НФТ в исследуемой группе была у 28 реципиентов из 58 (48,3%), в контрольной группе – 63,4% (71 реципиент). Было четыре случая ПНФТ, эти пациенты не были включены в исследуемую группу. 5-летняя выживаемость трансплантатов составила 82,8% (n = 48), в отличие от 87,5% (n=98) (ДСМ) (p>0,05). Уровень сывороточного креатинина через пять лет после трансплантации в среднем у реципиентов почек от АСД – 0,094(0,06)и 0,103(0,07) ммоль/л (от ДСМ) (p>0,05). ВЫВОДЫ. Восстановление и сохранение жизнеспособности донорских органов у внезапно умерших с критическим периодом асистолии с помощью экстракорпоральной перфузии in situ является многообещающим протоколом. Обязательным является применение тромболитиков и механического перфузионного удаления лейкотромбоагломератов, образующихся в период отсутствия кровообращения. Пятилетние результаты пересадки почек, полученных от АСД, с использованием экстракорпоральной перфузии in situ, не отличаются от результатов трансплантаций почек от ДСМ.
НАБЛЮДЕНИЯ ИЗ ПРАКТИКИ
Хронический лимфолейкоз (ХЛЛ) – самый частый вид лейкозов в Западной Европе. Несмотря на относительную частоту этого вида лейкоза, публикации о поражении почек при ХЛЛ встречаются редко. Нефробиопсии рутинно не выполняются этим больным при появлении нефротического синдрома или неясной почечной недостаточности, в результате о механизмах почечного поражения при ХЛЛ известно мало. К настоящему времени в литературе описано всего около 130 случаев гломерулярных и интерстициальных поражений почек при ХЛЛ, подтвержденных результатами нефробиопсий. Наиболее частой формой гломерулопатии, вызывающей нефротический синдром при ХЛЛ, является мембранно-пролиферативный гломерулонефрит, реже встречаются болезнь минимальных изменений, мембранозная нефропатия; фокально-сегментарный гломерулосклероз (ФСГС) является редкостью, и к настоящему времени опубликовано 6 случаев ФСГС, ассоциированного с ХЛЛ. Мы представляем клинический случай, описывающий пациента, страдавшего ХЛЛ, у которого развился нефротический синдром, вызванный ФСГС, успешно леченный ритуксимабом , а также литературный обзор по паранеопластическим гломерулопатиям, ассоциированных с ХЛЛ, проявляющимся нефротическим синдромом.
ПРОГРАММА НЕПРЕРЫВНОГО ПОСЛЕДИПЛОМНОГО ОБРАЗОВАНИЯ ПО НЕФРОЛОГИИ
Трансплантация почки (ТП) до недавнего времени считалась противопоказанной пациентам с терминальной почечной недостаточностью в исходе атипичного гемолитико-уремического синдрома (аГУС) из-за высокого риска рецидива основного заболевания и потери трансплантата. Однако в настоящее время разработаны новые подходы к профилактике и лечению рецидива аГУС в посттрансплантационном периоде, что способствовало значительному улучшению результатов ТП у этой категории больных. В статье рассматриваются принципы оценки риска рецидива аГУС после ТП, подбора органного донора, особенности иммуносупрессивной терапии, профилактики и лечения эпизодов аГУС у реципиентов ренального трансплантата.
ЮБИЛЕИ
УКАЗАТЕЛИ
ISSN 2541-9439 (Online)